近日,海思科創(chuàng)新藥研發(fā)迎新進(jìn)展,HSK16149膠囊申報(bào)上市、HSK31858片Ⅱ期臨床試驗(yàn)獲倫理批準(zhǔn)。目前海思科有16個(gè)創(chuàng)新藥(13個(gè)1類新藥)在研,3款1類新藥上市可期;麻醉新藥快速放量,License-in/out交易并行;23個(gè)品種過評(píng)(11個(gè)為國(guó)內(nèi)首家),8個(gè)品種中標(biāo)國(guó)家集采,3個(gè)新分類報(bào)產(chǎn)品種在審。
13款1類新藥在研,瞄準(zhǔn)3大千億市場(chǎng)
11月8日,海思科發(fā)布公告稱,1類新藥HSK16149膠囊上市申請(qǐng)獲國(guó)家藥監(jiān)局受理,擬用于周圍性神經(jīng)病理性疼痛的治療。11月16日,海思科發(fā)布公告稱,1類新藥HSK31858片Ⅱ期臨床試驗(yàn)獲得倫理批準(zhǔn),擬用于治療支氣管擴(kuò)張癥及急性肺損傷/急性呼吸窘迫綜合征引起的下呼吸道疾病。
海思科以創(chuàng)新藥研發(fā)、生產(chǎn)、銷售為核心業(yè)務(wù),致力于成為最受信賴的國(guó)際化創(chuàng)新藥企業(yè)。2022年上半年海思科研發(fā)投入3.47億元,同比增長(zhǎng)1.52%,研發(fā)投入占銷售收入的比重為27.82%。
目前海思科在研創(chuàng)新藥有16個(gè)(含1類13個(gè)、2類3個(gè)),聚焦于麻醉及鎮(zhèn)痛、糖尿病及并發(fā)癥、神經(jīng)痛以及腫瘤等疾病領(lǐng)域。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2021年中國(guó)城市公立醫(yī)院、縣級(jí)公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡(jiǎn)稱中國(guó)公立醫(yī)療機(jī)構(gòu))終端抗腫瘤和免疫調(diào)節(jié)劑、消化系統(tǒng)及代謝藥銷售規(guī)模均超過1700億元,神經(jīng)系統(tǒng)藥物銷售規(guī)模超過1000億元.
海思科主要?jiǎng)?chuàng)新藥情況
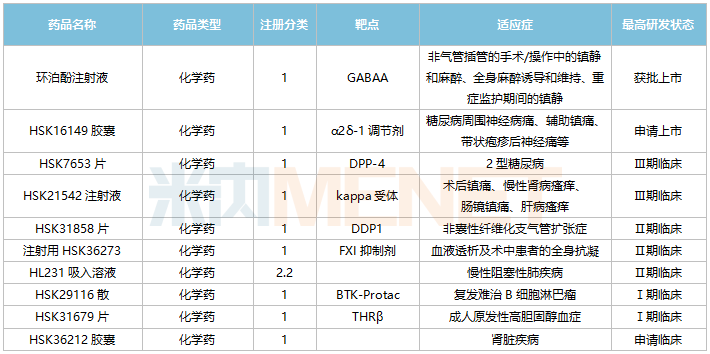
來源:米內(nèi)網(wǎng)中國(guó)臨床試驗(yàn)庫、公司公告
公司創(chuàng)新研發(fā)管線逐步進(jìn)入兌現(xiàn)期,目前α2δ-1調(diào)節(jié)劑HSK16149膠囊已申報(bào)上市;DPP-4抑制劑HSK7653片、kappa受體HSK21542注射液均處于Ⅲ期臨床階段;DPP1抑制劑HSK31858片、FXI抑制劑注射用HSK36273、HL231吸入溶液均處于Ⅱ期臨床階段。
3款1類新藥上市可期!HSK16149膠囊可以與鈣離子通道α2δ亞受體結(jié)合,首個(gè)申報(bào)上市的適應(yīng)癥為糖尿病周圍神經(jīng)痛,帶狀皰疹后神經(jīng)痛適應(yīng)癥處于Ⅲ期臨床階段。HSK7653是一款DPP-4長(zhǎng)效抑制劑,計(jì)劃于2022年底申報(bào)NDA,有望成為全球首款降糖藥雙周制劑。HSK21542注射液是鎮(zhèn)痛加止癢雙重作用的外周kappa阿片受體選擇性激動(dòng)劑,是公司首個(gè)國(guó)際化的fast follow新藥,開發(fā)適應(yīng)癥包括術(shù)后鎮(zhèn)痛、尿毒癥瘙癢、肝病瘙癢等。
環(huán)泊酚銷售額暴漲!拿下4筆License-in/out交易
環(huán)泊酚注射液是海思科首個(gè)進(jìn)入商業(yè)化階段的1類新藥,也是麻醉領(lǐng)域重磅創(chuàng)新藥,2021年11月獲納入2021版國(guó)家醫(yī)保目錄。以獲批上市作為“起點(diǎn)”,環(huán)泊酚注射液適應(yīng)癥持續(xù)拓展、國(guó)際化穩(wěn)步推進(jìn),目前在國(guó)內(nèi)已獲批非氣管插管的手術(shù)/操作中的鎮(zhèn)靜和麻醉、全身麻醉誘導(dǎo)和維持、重癥監(jiān)護(hù)期間的鎮(zhèn)靜等適應(yīng)癥;在美國(guó)直接開展Ⅲ期臨床研究,預(yù)計(jì)于2023年底申報(bào)上市。
適應(yīng)癥拓展與醫(yī)保助力下,環(huán)泊酚注射液市場(chǎng)迎來快速放量。財(cái)報(bào)顯示,2022年上半年環(huán)泊酚銷售數(shù)量約150萬支,已進(jìn)入900多家醫(yī)院,其中三甲以上醫(yī)院占比達(dá)55%;力爭(zhēng)全年目標(biāo)醫(yī)院覆蓋達(dá)到1400家左右,全年實(shí)現(xiàn)環(huán)泊酚銷售數(shù)量達(dá)400萬支以上。令人矚目的是,上半年公司麻醉產(chǎn)品銷售額實(shí)現(xiàn)1.29億元,同比增長(zhǎng)1602.52%。
除了自研產(chǎn)品的國(guó)際化,海思科還積極加強(qiáng)商務(wù)發(fā)展,自2021年開始加速推動(dòng)研發(fā)項(xiàng)目License-out和License-in,優(yōu)化商業(yè)合作充盈產(chǎn)品管線。
License-out方面,海思科海外控股子公司FTP-637項(xiàng)目出售給Foresite Capital,獲得6000萬美元首付款和最高1.2億美元的里程碑付款,彰顯公司研發(fā)實(shí)力與產(chǎn)品國(guó)際化潛力。FTP-637是一款TYK2抑制劑,全球首款TYK2抑制劑于2022年9月獲FDA批準(zhǔn)上市,為百時(shí)美施貴寶的氘可來昔替尼。
License-in方面,海思科先后引進(jìn)美國(guó)Starton用于腫瘤化療所致嘔吐的奧氮平透皮貼劑、美國(guó)Biosplice長(zhǎng)效治療骨關(guān)節(jié)炎的Lorecivivint、美國(guó)Aquestive治療“漸凍癥”的利魯唑口腔膜。
目前全球暫無奧氮平透皮貼劑獲批上市。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2021年中國(guó)公立醫(yī)療機(jī)構(gòu)終端奧氮平銷售規(guī)模超過20億元,同比增長(zhǎng)6.63%;2022年上半年其銷售規(guī)模超過10億元,同比下滑9.66%。利魯唑是FDA批準(zhǔn)的第一個(gè)漸凍癥藥物,2021年在中國(guó)公立醫(yī)療機(jī)構(gòu)終端銷售規(guī)模超過1億元,國(guó)內(nèi)已上市制劑包括利魯唑片、利魯唑膠囊、利魯唑口服混懸液。
23個(gè)品種過評(píng),仿制藥管線“收縮”?
仿制藥方面,海思科累計(jì)已有22個(gè)首仿藥獲批上市。隨著公司向創(chuàng)新藥轉(zhuǎn)型,仿制藥在研產(chǎn)品逐步減少。2022年至今海思科只提交了格列齊特緩釋片一款仿制藥的上市申請(qǐng),于7月5日獲CDE承辦。
公司僅剩3個(gè)新注冊(cè)分類仿制藥上市申請(qǐng)?jiān)趯彛唧w為利丙雙卡因乳膏、復(fù)方維生素注射液、格列齊特緩釋片,獲批生產(chǎn)后將視同通過一致性評(píng)價(jià)。隨著仿制藥品種數(shù)量不再新增、存量品種集采消化完畢,公司仿制藥業(yè)務(wù)將進(jìn)入穩(wěn)定發(fā)展?fàn)顟B(tài)。
目前,海思科已有23個(gè)品種通過/視同通過一致性評(píng)價(jià)。其中,11個(gè)品種為國(guó)內(nèi)首家過評(píng),聚普瑞鋅顆粒、復(fù)方氨基酸注射液(18AA-Ⅶ)、復(fù)方氨基酸(18AA)/葡萄糖(15%)電解質(zhì)注射液等3個(gè)品種為獨(dú)家過評(píng)。
海思科通過/視同通過一致性評(píng)價(jià)品種
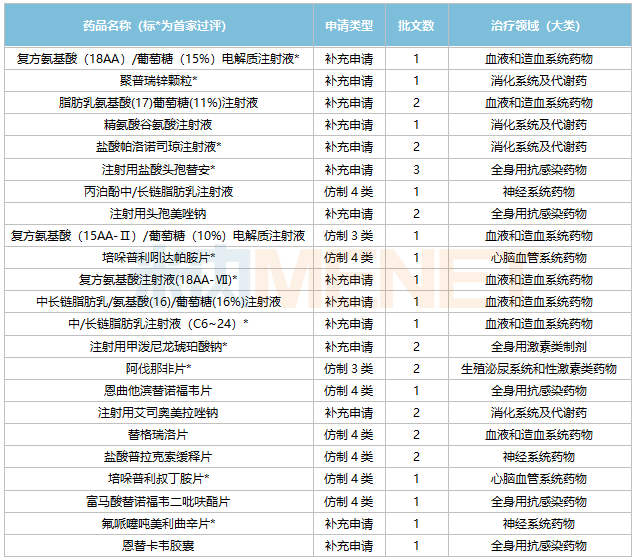
來源:米內(nèi)網(wǎng)中國(guó)申報(bào)進(jìn)度(MED)數(shù)據(jù)庫
從治療領(lǐng)域上看,23個(gè)品種主要集中在血液和造血系統(tǒng)藥物(7個(gè))、全身用抗感染藥物(5個(gè))。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2021年中國(guó)公立醫(yī)療機(jī)構(gòu)終端血液和造血系統(tǒng)藥物、全身用抗感染藥物銷售規(guī)模均超過1500億元。
在國(guó)家開展的第三、第四批集采中,海思科各有3個(gè)品種中標(biāo),第七批集采則有2個(gè)品種中標(biāo),累計(jì)8個(gè)品種中標(biāo)國(guó)家集采。其中,5個(gè)品種以一致性評(píng)價(jià)補(bǔ)充申請(qǐng)過評(píng),3個(gè)品種以新分類注冊(cè)批產(chǎn)并視同過評(píng)。
一致性評(píng)價(jià)補(bǔ)充申請(qǐng)方面,海思科還有6個(gè)品種在審,包括復(fù)方氨基酸注射液(20AA)、注射用醋酸卡泊芬凈、復(fù)方氨基酸注射液(18AA-Ⅸ)、磺達(dá)肝癸鈉注射液、富馬酸盧帕他定片、復(fù)方氨基酸注射液(18AA-Ⅶ)。其中,富馬酸盧帕他定片、復(fù)方氨基酸注射液(18AA-IX)沖刺首家過評(píng)。
數(shù)據(jù)來源:米內(nèi)網(wǎng)數(shù)據(jù)庫、公司公告注:米內(nèi)網(wǎng)《中國(guó)公立醫(yī)療機(jī)構(gòu)藥品終端競(jìng)爭(zhēng)格局》,統(tǒng)計(jì)范圍是:中國(guó)城市公立醫(yī)院、縣級(jí)公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院,不含民營(yíng)醫(yī)院、私人診所、村衛(wèi)生室;上述銷售額以產(chǎn)品在終端的平均零售價(jià)計(jì)算。

