中國(guó)醫(yī)藥化工網(wǎng)訊
近日,國(guó)家食品藥品監(jiān)督管理總局發(fā)布《2015年度藥品檢查報(bào)告》,公布了2015年藥品生產(chǎn)質(zhì)量管理規(guī)范(簡(jiǎn)稱(chēng)藥品GMP)認(rèn)證檢查、GMP跟蹤檢查、飛行檢查等7項(xiàng)檢查情況,共計(jì)檢查企業(yè)698家次。其中,藥品GMP認(rèn)證檢查數(shù)量較前兩年有所降低,但藥品生產(chǎn)企業(yè)的整改率同比提高近一倍。業(yè)內(nèi)專(zhuān)家紛紛表示,藥品生產(chǎn)質(zhì)量監(jiān)管力度明顯加強(qiáng),一批小、散、亂的藥品生產(chǎn)企業(yè)逐漸被淘汰,行業(yè)整合升級(jí)跡象顯現(xiàn)。
新版GMP成效明顯
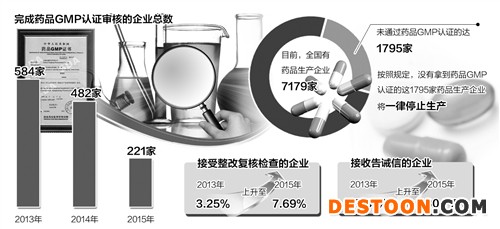
報(bào)告顯示,2015年國(guó)家食品藥品監(jiān)督管理總局食品藥品審核查驗(yàn)中心共接收藥品GMP認(rèn)證申報(bào)資料221份。其中,完成審核的企業(yè)總數(shù)由2013年的584家、2014年的482家降至2015年的221家,創(chuàng)下近3年的新低。
“去年完成審核的藥品生產(chǎn)企業(yè)數(shù)量同比下降幅度之所以大,與新版藥品GMP認(rèn)證有密切聯(lián)系。”國(guó)家食藥監(jiān)總局相關(guān)負(fù)責(zé)人介紹說(shuō),根據(jù)規(guī)定,國(guó)家食藥監(jiān)總局2011年3月啟動(dòng)了新版藥品GMP認(rèn)證,并要求血液制品、疫苗、注射劑等無(wú)菌藥品的生產(chǎn),應(yīng)在2013年12月31日前達(dá)到新版藥品GMP要求;其他類(lèi)別藥品的生產(chǎn)均應(yīng)在2015年12月31日前達(dá)到新版藥品GMP要求。未通過(guò)新版藥品GMP認(rèn)證的企業(yè)、生產(chǎn)車(chē)間一律停止生產(chǎn)。
在2015年藥品GMP認(rèn)證檢查中,共安排檢查224家次,其中212家藥品生產(chǎn)企業(yè)通過(guò)檢查,9家企業(yè)未通過(guò)。報(bào)告顯示,對(duì)無(wú)菌藥品生產(chǎn)風(fēng)險(xiǎn)控制不足、數(shù)據(jù)可靠性問(wèn)題、質(zhì)量管理體系無(wú)法保證產(chǎn)品的生產(chǎn)和質(zhì)量要求等是9家企業(yè)未能通過(guò)檢查的主要因素。
與舊版GMP相比,新版藥品GMP認(rèn)證更接近國(guó)際標(biāo)準(zhǔn),對(duì)企業(yè)的生產(chǎn)設(shè)備和管理水平要求也更高。尤其是對(duì)生產(chǎn)環(huán)境、設(shè)備設(shè)施、文件管理、風(fēng)險(xiǎn)控制等一系列流程提出了明確要求,為政府部門(mén)監(jiān)管和保障藥品質(zhì)量安全提供了著力點(diǎn)。
藥品監(jiān)管日趨嚴(yán)格
報(bào)告顯示,藥品GMP認(rèn)證檢查數(shù)量較前兩年有所降低,但接受整改復(fù)核檢查和接收告誡信的企業(yè)所占比例明顯上升,前者由2013年的3.25%上升至2015年的7.69%,后者則由2013年的17.81%上升至2015年的30.77%。
與此同時(shí),《2015年全國(guó)收回藥品GMP證書(shū)情況統(tǒng)計(jì)》顯示,2015年全國(guó)共有140家藥企的144張GMP證書(shū)被收回。國(guó)家食藥監(jiān)總局公布的數(shù)據(jù)顯示,目前,全國(guó)有藥品生產(chǎn)企業(yè)7179家,未通過(guò)藥品GMP認(rèn)證的達(dá)1795家。按照規(guī)定,沒(méi)有拿到“準(zhǔn)生證”的這1795家藥品生產(chǎn)企業(yè)將一律停止生產(chǎn)。
“新版藥品GMP認(rèn)證實(shí)施后,一定程度上促進(jìn)了醫(yī)藥行業(yè)重新洗牌。”中國(guó)醫(yī)藥[3.91% 資金 研報(bào)]保健品進(jìn)出口商會(huì)副會(huì)長(zhǎng)劉張林認(rèn)為,標(biāo)準(zhǔn)嚴(yán)格的認(rèn)證給藥企經(jīng)營(yíng)環(huán)境帶來(lái)了更大的考驗(yàn),有實(shí)力的大藥企紛紛出招力保拿到“準(zhǔn)生證”。
不過(guò),通過(guò)藥品GMP認(rèn)證并非意味著可以“一勞永逸”。隨著今年藥品GMP認(rèn)證下放到省級(jí)食藥監(jiān)局,省級(jí)GMP認(rèn)證檢查任務(wù)進(jìn)一步加大,藥企也開(kāi)始面臨更多的飛行檢查、跟蹤檢查、抽查檢查等運(yùn)動(dòng)式檢查,監(jiān)管力度也進(jìn)一步加強(qiáng)。據(jù)不完全統(tǒng)計(jì),截至5月底,通過(guò)飛行檢查,全國(guó)已有52家藥企被收回GMP認(rèn)證證書(shū)。
前不久,國(guó)家食藥監(jiān)總局食品藥品審核查驗(yàn)中心又公布了2016年藥品首批GMP跟蹤檢查的216家企業(yè)名單,多個(gè)省區(qū)市也公布了2016年GMP飛行檢查方案和工作重點(diǎn)。“216家企業(yè)的名單數(shù)量比去年增加了20%的跟蹤檢查企業(yè)數(shù)量,而這個(gè)數(shù)字在2017年很有可能會(huì)繼續(xù)增加,飛行檢查的力度還會(huì)增強(qiáng)。”天津市市場(chǎng)和質(zhì)量監(jiān)督管理委員會(huì)認(rèn)證中心工作人員王守斌表示,今后,飛行檢查的力度和嚴(yán)格程度必定會(huì)再上一個(gè)臺(tái)階。
行業(yè)將迎整合大潮
目前,嚴(yán)格的飛行檢查已經(jīng)成為藥品的常態(tài)監(jiān)管措施。在飛行檢查常態(tài)化、嚴(yán)格化之后,未通過(guò)認(rèn)證、被直接淘汰的藥企數(shù)量也隨之增加。
“很多未通過(guò)藥品GMP認(rèn)證的企業(yè)都是小企業(yè),因?yàn)闊o(wú)法負(fù)擔(dān)成本而放棄GMP認(rèn)證,部分中藥生產(chǎn)企業(yè)直接轉(zhuǎn)做保健品市場(chǎng),而很多靠生產(chǎn)批號(hào)過(guò)日子的小企業(yè)直接選擇退出市場(chǎng)。”北京鼎臣醫(yī)藥管理咨詢(xún)中心負(fù)責(zé)人史立臣認(rèn)為,對(duì)于那些擁有多個(gè)有價(jià)值的藥品批文的企業(yè),即使沒(méi)有通過(guò)新版GMP認(rèn)證,未來(lái)也可以與通過(guò)認(rèn)證、實(shí)力雄厚的企業(yè)并購(gòu)整合,實(shí)現(xiàn)共贏。而對(duì)于已經(jīng)順利拿到藥品GMP認(rèn)證證書(shū)的藥企,規(guī)范生產(chǎn)、提高藥品質(zhì)量才是根本。
值得注意的是,產(chǎn)能過(guò)剩、成本上升等問(wèn)題始終制約著我國(guó)醫(yī)藥行業(yè)的發(fā)展。當(dāng)前,我國(guó)藥品生產(chǎn)企業(yè)整體上小、散、亂的格局尚未根本改變,市場(chǎng)上藥品同質(zhì)化現(xiàn)象比較嚴(yán)重,由此造成的生產(chǎn)經(jīng)營(yíng)不規(guī)范、低水平重復(fù)和過(guò)度競(jìng)爭(zhēng)是引發(fā)藥品質(zhì)量安全事件的主要原因。
對(duì)此,業(yè)內(nèi)專(zhuān)家認(rèn)為,從行業(yè)發(fā)展需要來(lái)看,新版藥品GMP認(rèn)證能“倒逼”藥品生產(chǎn)企業(yè)規(guī)范產(chǎn)品、提升質(zhì)量,淘汰落后企業(yè),為行業(yè)龍頭和上市企業(yè)提供更多整合升級(jí)的機(jī)會(huì)。未來(lái),國(guó)內(nèi)藥企也不能再依靠低價(jià)格低成本競(jìng)爭(zhēng),而要在合規(guī)的基礎(chǔ)上提高藥品質(zhì)量,提升企業(yè)競(jìng)爭(zhēng)力??傊?,隨著新版藥品GMP認(rèn)證加速推進(jìn)以及各項(xiàng)政策措施協(xié)調(diào)配合,我國(guó)藥品質(zhì)量安全保障能力將進(jìn)一步提升。



 110102000668(1)號(hào)
110102000668(1)號(hào)