日前,康緣藥業(yè)發(fā)布公告稱,近日收到國家藥品監(jiān)督管理局簽發(fā)的九味疏風平喘顆?!端幬锱R床試驗批準通知書》,同意其進行臨床試驗。目前,國內已上市且功能主治為支氣管哮喘的中藥主要有桂龍咳喘寧膠囊、如意定喘片、小青龍顆粒、雙黃平喘顆粒等,主要用于寒哮、熱哮及氣陰兩虛所致哮喘。九味疏風平喘顆粒屬國內外首創(chuàng)用于治療“風哮”的藥物,為中藥創(chuàng)新藥1.1 類,如能通過臨床研究證實其療效并最終獲批上市,將填補“風哮”用藥的空白。資料顯示,截至目前,九味疏風平喘顆粒累計研發(fā)投入約為816.15 萬元。
近年來,國家大力鼓勵中藥創(chuàng)新,針對中藥研發(fā)出臺了多項扶持政策。自新修訂的《藥品注冊管理辦法》、《中藥注冊分類及申報資料要求》等一系列符合中藥特點的規(guī)章及相關技術指導原則相繼發(fā)布實施以來,中藥創(chuàng)新活力和潛能不斷釋放,中藥新藥研發(fā)動力大增,中藥新藥質量得到提升。
從國家醫(yī)保局連續(xù)開展的4次國家醫(yī)保藥品目錄調整工作看,目前已累計有507個藥品新增進入全國醫(yī)保支付范圍。其中,有8個為2017年以來上市的中藥新藥,占近五年中藥新藥獲批上市數量的47.06%。2021年國家醫(yī)保藥品目錄調整,67個談判新增藥品中有3個為中藥新藥,為患者臨床用藥提供了更多新選擇。
上市量超過去4年總和
康緣、天士力、以嶺、方盛領銜
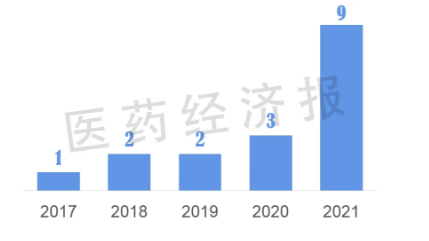
國家藥監(jiān)局官網數據顯示,2017年至今共有17個中藥新藥獲批上市(見表1)。從獲批數量看,2017-2021年中藥新藥上市數量呈遞增趨勢。今年以來,國家藥監(jiān)局在通過特別審批程序應急批準清肺排毒顆粒、化濕敗毒顆粒、宣肺敗毒顆粒的基礎上,又批準了6個中藥新藥上市。截至12月12日,2021年共有9個中藥新藥上市,為近5年獲批數量最多的一年,獲批數量超過去4年之和(見圖1)。
表1 近5年中藥新藥獲批上市情況
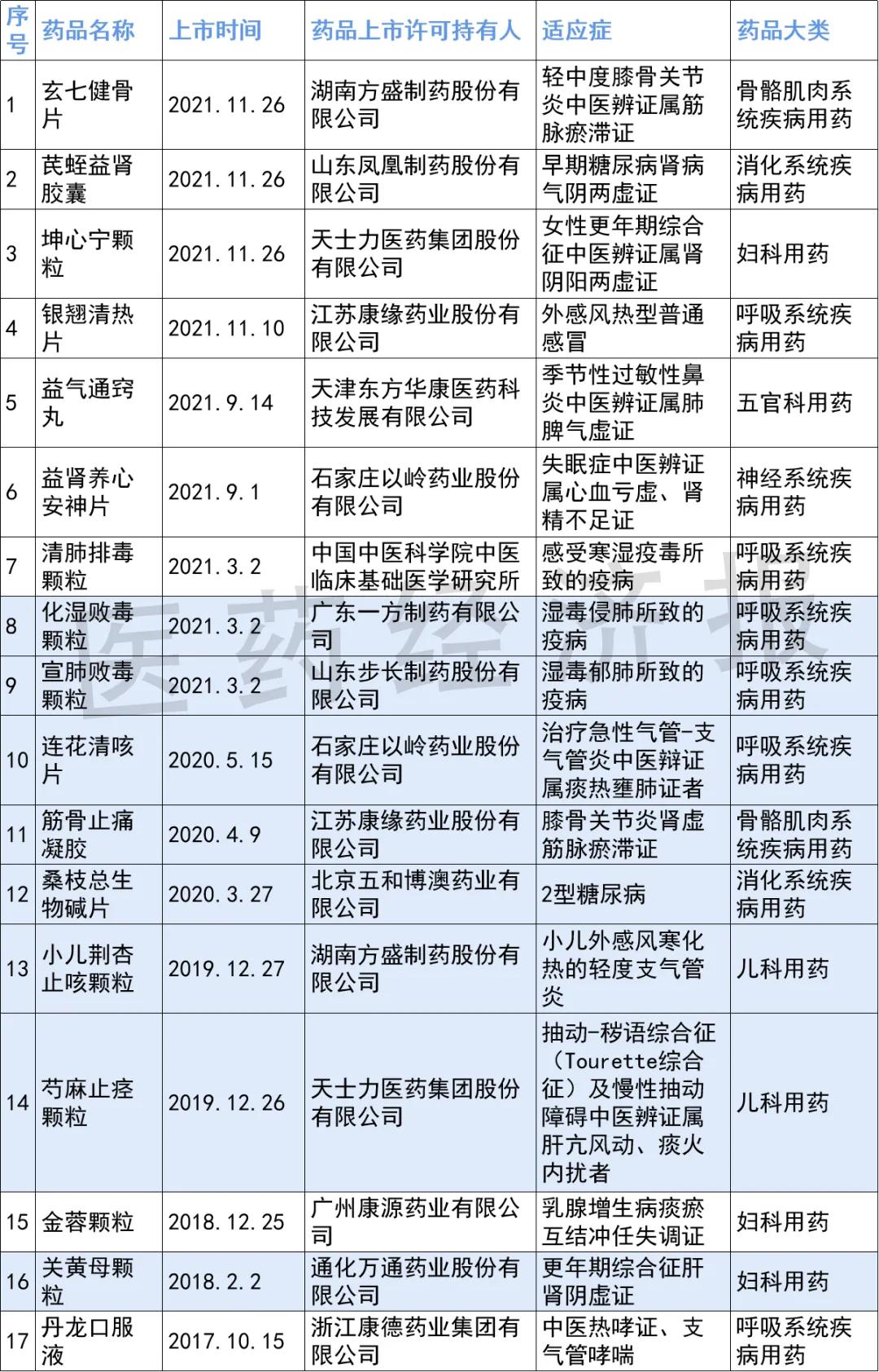
注:藍底色為通過談判調入國家醫(yī)保藥品目錄的中藥新藥。
?。▉碓矗簢宜幈O(jiān)局官網、米內網數據庫)
圖1 2017-2021年中藥新藥獲批數量
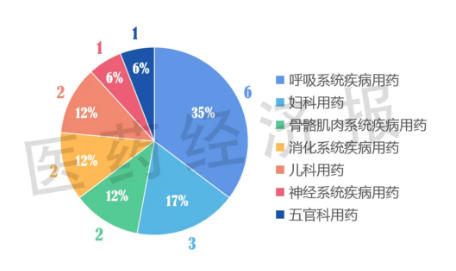
從用藥分類看,近五年上市的中藥新藥主要集中在呼吸系統(tǒng)、婦科、骨骼肌肉系統(tǒng)、消化系統(tǒng)、兒科、神經系統(tǒng)以及五官科疾病用藥領域(見圖2)。其中,呼吸系統(tǒng)疾病中藥新藥上市數量最多,為6個,占比達35%??稻壦帢I(yè)的銀翹清熱片既是2020年7月1日新的中藥注冊分類實施以來首個獲批上市的1.1類中藥創(chuàng)新藥,也是繼2016年金花清感顆粒獲批后,近5年來首個獲批上市的感冒中藥創(chuàng)新藥。
圖2 2017-2021年上市中藥新藥分類及占比
為了鼓勵藥品創(chuàng)新、提升藥品質量,開展藥品上市許可持有人制度試點成為我國藥品審評審批制度改革的一項重要內容。在2017年至今獲批的17個中藥新藥中,江蘇康緣藥業(yè)股份有限公司、天士力醫(yī)藥集團股份有限公司、石家莊以嶺藥業(yè)股份有限公司和湖南方盛制藥股份有限公司均有2款中藥新藥獲批上市,為獲批數量最多的藥品上市許可持有人。
而部分中藥新藥在中國城市實體藥店終端也已經取得了不錯的銷量。據米內網最新數據顯示,在中國公立醫(yī)療機構終端,桑枝總生物堿片2021年上半年銷售額暴增9650%,而連花清咳片上半年的銷售額達到211萬元。
中成藥進醫(yī)保意愿強烈
新藥研發(fā)投入略顯不足
醫(yī)保談判作為中成藥放量的重要催化劑,是銜接中藥研發(fā)和商業(yè)化的重要一環(huán)。雖然納入醫(yī)保目錄后,企業(yè)會大幅讓利,但在量價博弈中,藥品往往能享受進院的紅利和新增患者需求的提升,最終通過以量換價為品種帶來增量貢獻。
回顧近三年中成藥進入國家醫(yī)保藥品目錄的情況可以發(fā)現,2019-2021年分別有23個、40個和3個中成藥通過談判進入國家醫(yī)保目錄。通過調整,2020年和2021年國家醫(yī)保藥品目錄中的中成藥數量均達到1374種,占比近50%。且2020年和2021年通過談判,共新增8個中藥新藥,占近五年中藥新藥獲批上市數量的47.06%。由此可見,中成藥進醫(yī)保的意愿十分強烈。
然而,與中成藥進醫(yī)保意愿形成鮮明對比的是,盡管近年來中藥新藥研發(fā)熱情逐漸高漲,但與化藥、生物藥相比,中藥新藥研發(fā)投入依然略顯平淡。
財報數據顯示,2021年前三季度73家中藥上市企業(yè)中,僅白云山、以嶺藥業(yè)、天士力、華潤三九、康緣藥業(yè)、步長藥業(yè)、濟川藥業(yè)、云南白藥、桂林三金、康恩貝、紅日藥業(yè)、亞寶藥業(yè)、中恒集團等13家中藥上市企業(yè)研發(fā)費用超過1億元(見表2)。雖然多家企業(yè)2021年前三季度研發(fā)投入遠超去年同期,增幅翻倍,甚至高達400%以上,但與傳統(tǒng)化藥企業(yè)動輒幾十億元的研發(fā)費用相比,依然不可同日而語。
表2 研發(fā)投入超億元中藥上市企業(yè)情況
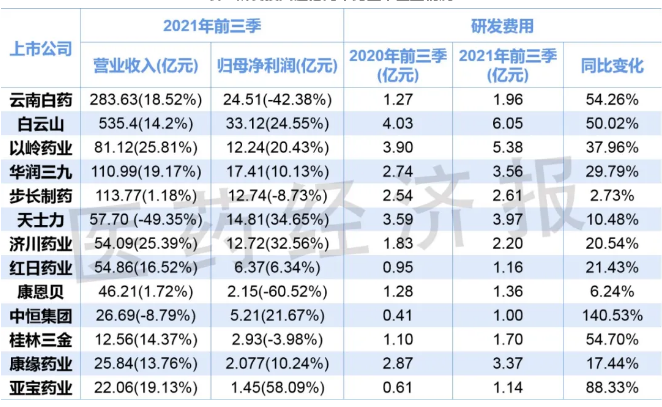
(注:括號內為同比變化,來源:Choice數據)
就中藥研發(fā)具體品種而言,主要聚焦于心腦血管、呼吸、消化、內分泌、婦兒等中醫(yī)藥優(yōu)勢特色治療領域。以嶺藥業(yè)今年上半年申報的2項中藥新藥益腎養(yǎng)心安神片、蘇夏解郁除煩膠囊,用于失眠癥的益腎養(yǎng)心安神片已于今年9月上市。而今年5月申報的小兒連花清感顆粒,已取得國家藥品監(jiān)督管理局藥物臨床試驗批準通知書,2期臨床研究正在積極籌備,有望助其在呼吸及兒科領域開拓新的市場。
表3 以嶺藥業(yè)已獲批準進入臨床的中藥品種研發(fā)進展

中藥新藥研發(fā)陣痛不斷
院內制劑轉化為破局最佳捷徑
今年初發(fā)布的《國民經濟和社會發(fā)展第十四個五年規(guī)劃和2035年遠景目標綱要》,全方位擘畫了國家今后五年以及到2035年的行動安排。其中提到,“加強古典醫(yī)籍精華的梳理和挖掘,建設中醫(yī)藥科技支撐平臺,改革完善中藥審評審批機制,促進中藥新藥研發(fā)保護和產業(yè)發(fā)展。強化中藥質量監(jiān)管,促進中藥質量提升。”不過,有專家認為,要著力解決這一問題,還需要一套完整、切實可行且可量化的中藥質量標準。
就目前中藥新藥研發(fā)的狀況來看,處方用量大多依據藥典的規(guī)定,亦有根據劑型、制劑量、服用量確定藥物用量的,少數新藥復方制劑通過了1期臨床試驗后才確定服用劑量。北京中醫(yī)藥大學國家中醫(yī)藥發(fā)展與戰(zhàn)略研究院副研究員鄧勇直言,多數藥材劑量的標定缺乏科學性、規(guī)范性,也缺乏嚴格、合理的篩選。“中藥材及其飲片的質量是中藥新藥開發(fā)的前提和基礎,在我國目前的中藥材供應中還存在諸多問題。有些中藥材缺少產地來源、主要成分含量及采收時間標記,存在成分含量差異大、農藥殘留及重金屬超標等問題。另外,不同批次的產品所投原料來源也不同,勢必影響成藥質量的安全性和穩(wěn)定性。”而在重慶藥物研究所中醫(yī)藥產業(yè)研究員李旭看來,基礎研究和創(chuàng)新能力薄,科技含量較低,則是制約中藥現代化的關鍵問題。
如何破局?鄧勇建議,中藥的新藥開發(fā)研制應重視醫(yī)院中藥制劑,發(fā)揮其特點和作用,從中發(fā)掘出一些組方合理、療效確切、具有廣闊市場前景的品種。避免盲目尋找處方來源,縮短新藥開發(fā)周期,降低研究費用,是進行中藥新藥開發(fā)的捷徑之一。
不過,將院內中藥制劑轉化為新藥還存在不小的挑戰(zhàn)。比如,醫(yī)院制劑的適應癥寬泛、臨床定位不明確,療效往往缺乏有說服力的證據,其有效性就無從談起,這是制約其向新藥轉化的最主要的瓶頸問題。再加上當前新藥審評標準越來越高,雖然標準提高是保障新藥研發(fā)質量的關鍵與核心,但如何充分體現出中藥的特點、滿足臨床需求的中藥新藥如何盡快獲批,依然待解。具體來看,就是要保持中醫(yī)藥的療效優(yōu)勢與現代藥品審評要求、傳統(tǒng)用藥模式與現代審評需求的平衡關系。
為了打破院內中藥制劑轉化為新藥的瓶頸問題,鄧勇認為,“一方面,可以加強醫(yī)院信息系統(tǒng)建設,將療效觀察與患者隨訪的信息納入,從真實世界研究的角度,提供療效證據。設立規(guī)范的臨床研究,提供RCT證據;另一方面,應該以療效和安全性為根本出發(fā)點和落腳點,避免在工藝、質控上過分教條,可引領性地構建適合中藥特點的新藥開發(fā)新模式,建立以臨床為導向的藥物評價新方法,加快推進經典名方和名優(yōu)中成藥現代開發(fā)關鍵技術的突破。”



