一批械企被處罰,產(chǎn)品兩年不得掛網(wǎng)
5月7日,四川省藥械集中采購及醫(yī)藥價格監(jiān)管平臺發(fā)布《關于公布違規(guī)申報掛網(wǎng)的醫(yī)用耗材企業(yè)相關產(chǎn)品處理結(jié)果(第一批)的通知》,對違規(guī)企業(yè)的一批高值、低值耗材、診斷試劑予以降價、撤網(wǎng)處理。
據(jù)賽柏藍器械觀察,去年8月,四川省藥械招標采購服務中心發(fā)布《關于調(diào)整醫(yī)用耗材和體外診斷試劑掛網(wǎng)目錄范圍的通知》,具有醫(yī)療器械注冊證或備案憑證的全部體外診斷試劑,均被納入掛網(wǎng)目錄范圍。
根據(jù)《四川省醫(yī)藥機構醫(yī)用耗材集中采購實施方案》,已掛網(wǎng)產(chǎn)品申報企業(yè)主動根據(jù)最新外省最低參考價格進行降價,并在30天內(nèi)向省藥招中心提交價格信息;未及時更新并申報的,按核實后的外省實際最低參考價下調(diào)10%作為聯(lián)動參考價。
企業(yè)不予確認的,取消該產(chǎn)品掛網(wǎng)資格,自取消之日起兩年內(nèi)不再接受該產(chǎn)品的掛網(wǎng)申請。同時將有關違規(guī)情況納入該省藥品和醫(yī)用耗材集中采購信用評價和考核相關管理辦法的有關規(guī)定進行處理。
今年1月,四川省發(fā)布整改公告稱,將開展掛網(wǎng)藥械產(chǎn)品申報情況計算機校驗及人工復核,對凡存在瞞報全國最低價、不足五省價掛網(wǎng)、未按規(guī)定完成原四川流水號與國家醫(yī)保耗材編碼映射等違規(guī)行為的醫(yī)藥企業(yè),給予信用評級、暫停掛網(wǎng)和撤網(wǎng)等處理。
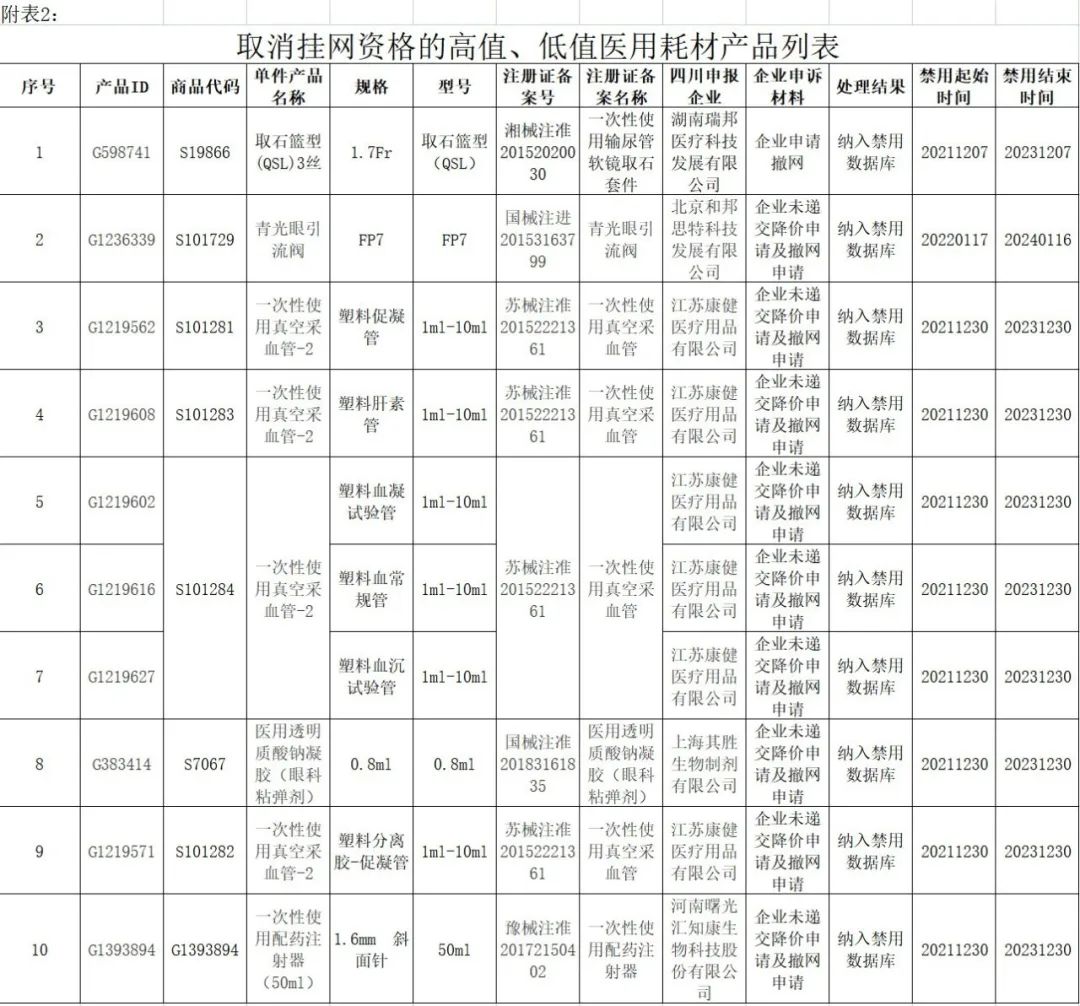
根據(jù)最新通知內(nèi)容,在此次核查工作中,共有15家企業(yè)的123個耗材、試劑產(chǎn)品存在問題,予以降價或撤網(wǎng)處罰。
其中,100條高值、低值醫(yī)用耗材產(chǎn)品和2條體外診斷試劑產(chǎn)品接受降價處罰,在原陽光采購平臺歷史最低采購價的基礎上,下浮10%作為最新掛網(wǎng)價;不愿接受降價處罰和未遞交相關澄清材料的10條醫(yī)用耗材和11條體外診斷試劑產(chǎn)品,被取消掛網(wǎng)資格,自取消之日起兩年內(nèi)不能掛網(wǎng)。
被取消掛網(wǎng)資格的產(chǎn)品包括一次性使用輸尿管軟鏡取石套件、青光眼引流閥、一次性使用真空采血管、醫(yī)用透明質(zhì)酸鈉凝膠(眼科粘彈劑)、一次性使用配藥注射器、人類免疫缺陷病毒抗體檢測試劑盒(膠體金法)、乙型肝炎病毒核心抗體檢測試劑盒(酶聯(lián)免疫法)等。
耗材、試劑,全國最低價聯(lián)動
實施耗材、體外診斷試劑最低價掛網(wǎng)的不只四川省。
4月25日,山東省藥械集中采購平臺發(fā)布《關于開展山東省醫(yī)用耗材和體外診斷試劑產(chǎn)品價格聯(lián)動的通知》,包括體外診斷試劑在內(nèi)的省平臺掛網(wǎng)產(chǎn)品,將價格聯(lián)動全國現(xiàn)行省級最低中標或掛網(wǎng)價。
《通知》指出,省平臺掛網(wǎng)產(chǎn)品價格聯(lián)動全國現(xiàn)行省級最低中標或掛網(wǎng)價,由企業(yè)自行申報。填報時間自2022年4月26日至2022年5月20日。
對于企業(yè)不承諾、不接受聯(lián)動省級最低中標或掛網(wǎng)價、經(jīng)查實提交虛假價格信息的產(chǎn)品,省平臺將予以撤網(wǎng),兩年內(nèi)不得重新掛網(wǎng)。應申報而未申報全國省級最低中標或掛網(wǎng)價的,視為不接受聯(lián)動省級最低中標或掛網(wǎng)價。
去年9月,山東省開展醫(yī)用耗材和體外診斷試劑產(chǎn)品掛網(wǎng)申報工作時也曾明確要求,醫(yī)用耗材和體外診斷試劑申報價格應是本產(chǎn)品全國現(xiàn)行省級掛網(wǎng)最低價,無省級價格信息的產(chǎn)品企業(yè)自行申報價格,進備選庫供醫(yī)療機構采購議價時參考。
除掛網(wǎng)采購外,全國多省、省際聯(lián)盟帶量采購中,也陸續(xù)出現(xiàn)低價聯(lián)動采購模式。
5月6日,福建省醫(yī)保局發(fā)布《福建省第三批醫(yī)用耗材集中帶量采購公告(第1號)》,將對冠脈導引導管類、冠脈導引導絲類、彈簧圈類、壓力泵類、圈套器(息肉勒除器)等5種耗材開展集中帶量采購。
其中明確,報價不得高于本企業(yè)同產(chǎn)品的省內(nèi)現(xiàn)行采購價格、全國最低價、全國其他地市級(含聯(lián)盟)及以上集中采購(含帶量采購)價格,中選耗材在履行合同中,如同產(chǎn)品在全國其他地市級(含聯(lián)盟)及以上集中采購(含帶量采購)中產(chǎn)生更低中選價,價格須相應聯(lián)動。
5月1日,京津冀“3+N”聯(lián)盟骨科創(chuàng)傷類醫(yī)用耗材帶量聯(lián)動采購中選結(jié)果在天津落地執(zhí)行。本次骨科創(chuàng)傷類醫(yī)用耗材集中帶量采購方式為帶量聯(lián)動、雙向選擇,即依據(jù)采購主體使用需求,參照市場總體價格水平,綜合質(zhì)量等因素,聯(lián)動河南等十二省骨科創(chuàng)傷類醫(yī)用耗材聯(lián)盟帶量采購價格。
此前河南12省聯(lián)盟骨科創(chuàng)傷集采中曾明確要求,同一產(chǎn)品如在國家或其他省級帶量采購中形成新的低價,其中選價格生效以后,本次采購尚未執(zhí)行的采購量,按新的中選價格執(zhí)行。29省骨科創(chuàng)傷耗材實現(xiàn)了最大規(guī)模的價格聯(lián)動。
通過報價環(huán)節(jié)和落地執(zhí)行環(huán)節(jié)的雙重低價聯(lián)動,確保耗材集采降價成果的全國共享,已經(jīng)成為集采規(guī)則的一環(huán)。
不難看出,經(jīng)過前期的摸索,耗材掛網(wǎng)采購、集中帶量采購降價步伐加快,效率正在提升。未來市場對高性價比器械產(chǎn)品的傾斜將更加明顯,企業(yè)必須跟緊節(jié)奏,加快掌握核心、前沿技術,降本增效。
附件: