我國仿制藥一致性評價工作在2012年啟動,2016年出臺的289目錄標志著進入全力推進階段……至今十年,越來越多細則落地,一致性評價工作已邁向成熟階段。截至2022年12月31日(按NMPA批準日期統(tǒng)計),已通過一致性評價(含視同過評)的受理號達5573個,涉及藥品4013個(按產(chǎn)品名+企業(yè)統(tǒng)計)。揚子江藥業(yè)、齊魯制藥已過評產(chǎn)品數(shù)量超過了100個,斷層式領先,正大制藥暫列TOP3,科倫藥業(yè)與石藥控股則在全力追趕。
圖1:近五年已通過一致性評價的受理號情況
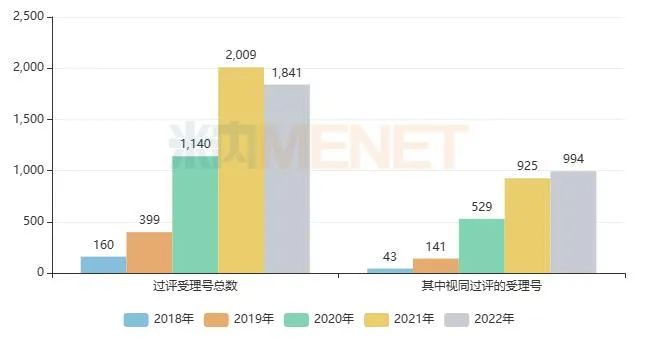
來源:米內網(wǎng)中國申報進度(MED)數(shù)據(jù)庫
米內網(wǎng)數(shù)據(jù)顯示,從近五年過評的受理號情況來看,2020年起每年均超過1000個,2021年暫為峰值(超過2000個)。從趨勢來看,按新分類視同過評的受理號越來越多,2022年的占比已超過53%,高端仿制藥已逐漸成為市場主力。一致性評價是優(yōu)勝劣汰的過程,只有高質量的仿制藥才能最終贏得市場的肯定。
四大類藥物過評潮火熱,8個超10億產(chǎn)品受熱捧
表1:截至2022年已過評的產(chǎn)品分布TOP10大類
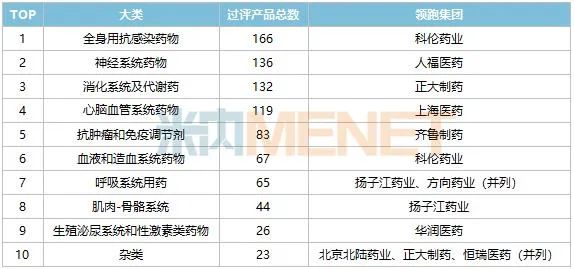
來源:米內網(wǎng)中國申報進度(MED)數(shù)據(jù)庫
已過評的全身用抗感染藥物主要集中在4個亞類,其中全身用抗細菌藥占了120個??苽愃帢I(yè)是該大類的過評領跑集團,已過評產(chǎn)品涉及全身用抗細菌藥24個、全身用抗病毒藥4個、全身用抗真菌藥3個。
已過評的神經(jīng)系統(tǒng)藥物主要集中在7個亞類,其中精神安定藥占了36個、精神興奮藥占了35個。人福醫(yī)藥是該大類的過評領跑集團,已過評產(chǎn)品涉及麻醉劑6個、止痛藥6個、精神安定藥3個、精神興奮藥3個、抗癲癇藥2個。
已過評的消化系統(tǒng)及代謝藥主要集中10個亞類,其中糖尿病用藥占了47個。正大制藥(含南京正大天晴制藥、正大天晴藥業(yè)集團、江蘇正大清江制藥等)是該大類的過評領跑集團,已過評產(chǎn)品涉及糖尿病用藥7個、止吐藥和止惡心藥3個、治療與胃酸分泌相關疾病的藥物3個、維生素類2個、止瀉藥及腸道抗炎/抗感染藥2個。
已過評的心腦血管系統(tǒng)藥物主要集中在4個亞類,其中高血壓用藥占了75個。上海醫(yī)藥是該大類的過評領跑集團,已過評產(chǎn)品涉及高血壓用藥12個、心臟病治療用藥4個、血脂調節(jié)劑2個、腦血管治療用藥1個。
表2:截至2022年過評熱度最高的TOP10產(chǎn)品
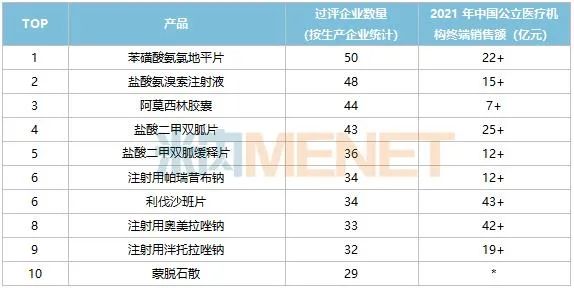
注:銷售額低于1億元用*表示
來源:米內網(wǎng)綜合數(shù)據(jù)庫
過評企業(yè)數(shù)量最多的TOP10產(chǎn)品有8個2021年在中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機構)終端的銷售額超10億元。
苯磺酸氨氯地平片熱度最高,已有50家生產(chǎn)企業(yè)通過了一致性評價,恒瑞、白云山、康緣藥業(yè)、宜昌東陽光、重慶藥友等國內明星企業(yè)均有涉足。
值得注意的是,阿莫西林膠囊、鹽酸二甲雙胍片、注射用奧美拉唑鈉目前擁有批文的企業(yè)數(shù)量超過100家,但已過評的企業(yè)占比不到40%。隨著時間推移,越來越多省市對未過評產(chǎn)品采取撤網(wǎng)、停止采購等舉措,或將有一批藥品陸續(xù)被市場“淘汰”。
最新過評TOP10集團出爐!揚子江、齊魯斷層式領先
表3:截至2022年過評產(chǎn)品數(shù)量TOP10集團
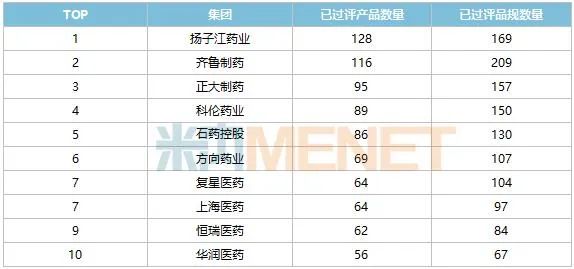
來源:米內網(wǎng)中國申報進度(MED)數(shù)據(jù)庫
揚子江藥業(yè)首個過評產(chǎn)品在2018年獲批(馬來酸依那普利片),2020年起進入過評井噴期,截至2022年年底共有128個產(chǎn)品過評,為過評榜TOP1企業(yè)。過評產(chǎn)品分布在12個大類,其中全身用抗感染藥物最多占25個,神經(jīng)系統(tǒng)藥物、抗腫瘤和免疫調節(jié)劑、消化系統(tǒng)及代謝藥、心腦血管系統(tǒng)藥物、呼吸系統(tǒng)用藥、肌肉-骨骼系統(tǒng)以及血液和造血系統(tǒng)藥物均有超過10個產(chǎn)品過評。
表4:揚子江藥業(yè)已過評的產(chǎn)品情況
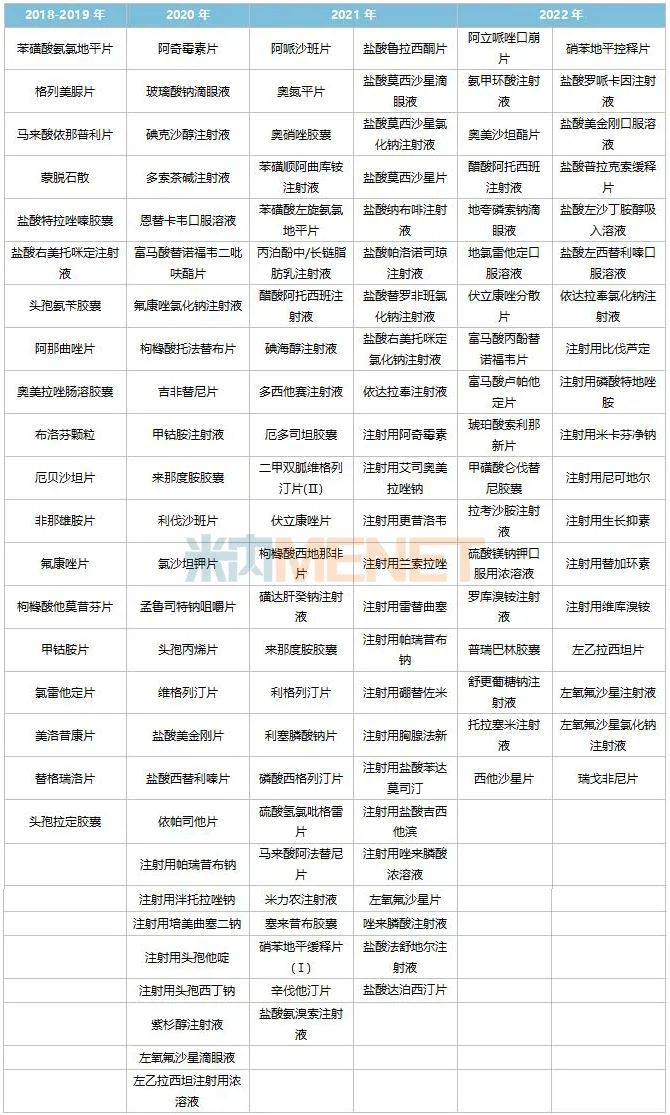
來源:米內網(wǎng)中國申報進度(MED)數(shù)據(jù)庫
揚子江藥業(yè)目前已有30個產(chǎn)品拿下了首家過評,涉及阿那曲唑片、奧美拉唑腸溶膠囊、奧硝唑膠囊、布洛芬顆粒、厄多司坦膠囊、恩替卡韋口服溶液、伏立康唑分散片、氟康唑氯化鈉注射液、富馬酸盧帕他定片、格列美脲片、枸櫞酸他莫昔芬片、甲鈷胺片、甲鈷胺注射液、利塞膦酸鈉片、馬來酸依那普利片、舒更葡糖鈉注射液、頭孢丙烯片、鹽酸特拉唑嗪膠囊、鹽酸右美托咪定注射液、依帕司他片、注射用雷替曲塞、注射用磷酸特地唑胺、注射用尼可地爾、注射用頭孢他啶、注射用頭孢西丁鈉、注射用維庫溴銨、紫杉醇注射液、左氧氟沙星滴眼液、左氧氟沙星注射液、瑞戈非尼片。
作為國內藥企第一梯隊的揚子江藥業(yè)不僅產(chǎn)品線豐富,研發(fā)實力也是行業(yè)前列,有100多個過評產(chǎn)品作為基石,集團在國采之路如魚得水,從最早的4+7試點一路走到第七批,揚子江藥業(yè)都積極參與,總中標產(chǎn)品數(shù)量已達42個。
齊魯制藥的首個過評產(chǎn)品在2017年獲批(吉非替尼片),截至2022年年底共有116個產(chǎn)品過評。過評產(chǎn)品分布在11個大類,其中抗腫瘤和免疫調節(jié)劑占29個(注射用培美曲塞二鈉有2家子公司過評),全身用抗感染藥物占26個,神經(jīng)系統(tǒng)藥物、消化系統(tǒng)及代謝藥各占10個以上。
表5:齊魯制藥已過評的產(chǎn)品情況
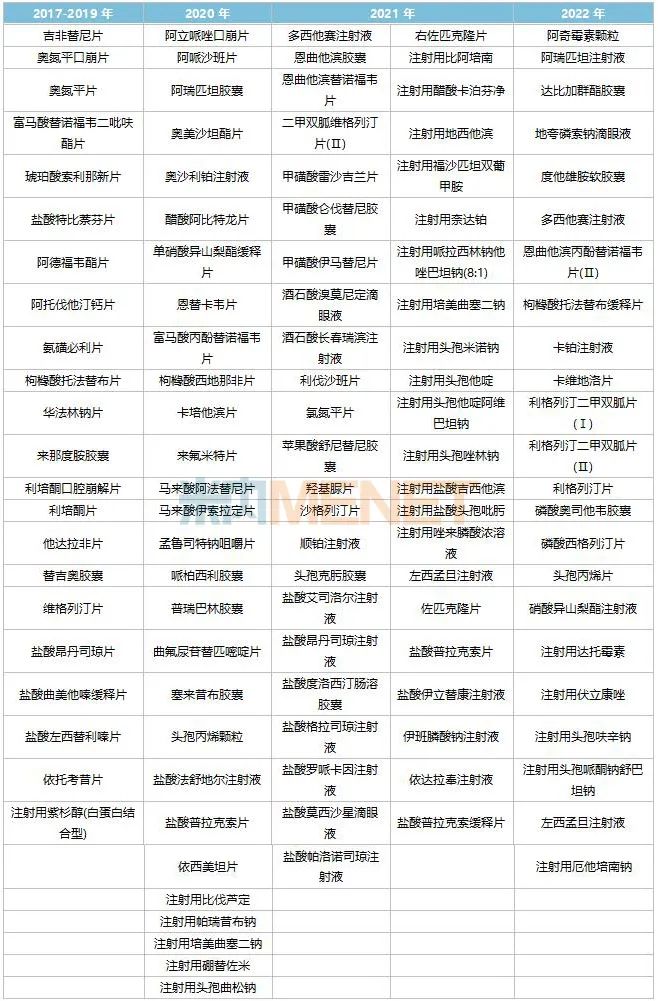
來源:米內網(wǎng)中國申報進度(MED)數(shù)據(jù)庫
齊魯制藥目前已有46個產(chǎn)品拿下首家過評,涉及吉非替尼片、奧氮平口崩片、鹽酸特比萘芬片、阿德福韋酯片、氨磺必利片、華法林鈉片、來那度胺膠囊、利培酮口腔崩解片、鹽酸昂丹司瓊片、鹽酸曲美他嗪緩釋片、鹽酸左西替利嗪片、依托考昔片、阿瑞匹坦膠囊、奧沙利鉑注射液、單硝酸異山梨酯緩釋片、卡培他濱片、來氟米特片、馬來酸伊索拉定片、哌柏西利膠囊、普瑞巴林膠囊、曲氟尿苷替匹嘧啶片、頭孢丙烯顆粒、鹽酸法舒地爾注射液、依西美坦片、注射用比伐蘆定、恩曲他濱膠囊、二甲雙胍維格列汀片(Ⅱ)、甲磺酸雷沙吉蘭片、酒石酸溴莫尼定滴眼液、羥基脲片、順鉑注射液、鹽酸艾司洛爾注射液、鹽酸昂丹司瓊注射液、鹽酸格拉司瓊注射液、鹽酸伊立替康注射液、注射用比阿培南、注射用頭孢他啶阿維巴坦鈉、注射用鹽酸頭孢吡肟、注射用唑來膦酸濃溶液、左西孟旦注射液、阿瑞匹坦注射液、枸櫞酸托法替布緩釋片、卡鉑注射液、卡維地洛片、硝酸異山梨酯注射液、注射用厄他培南鈉。
齊魯制藥從聯(lián)盟擴圍階段開始參與國采,第五批及第七批中標產(chǎn)品數(shù)量激增,分別達11個、16個產(chǎn)品。齊魯制藥總中標產(chǎn)品數(shù)達49個,“集采中標大戶”實至名歸。
正大制藥暫列過評集團TOP3,但與緊跟其后的科倫藥業(yè)、石藥控股之間尚未拉開足夠的差距,接下來的排位之爭或將出現(xiàn)新變數(shù)。
2017年9月,正大天晴藥業(yè)集團的富馬酸替諾福韋二吡呋酯片4類仿制獲批上市視同過評,成為了正大制藥首個過評的產(chǎn)品,截至2022年年底集團共有95個產(chǎn)品過評。過評產(chǎn)品分布在11個大類,其中抗腫瘤和免疫調節(jié)劑占22個、消化系統(tǒng)及代謝藥占17個、全身用抗感染藥物占17個。正大制藥也是國采積極分子,從最早的4+7試點一路走到第七批國采,總中標產(chǎn)品數(shù)量為41個,排在揚子江藥業(yè)之后。
科倫藥業(yè)首個過評產(chǎn)品在2018年2月獲批(草酸艾司西酞普蘭片),截至2022年年底集團共有89個產(chǎn)品過評。過評產(chǎn)品分布在11個大類,其中全身用抗感染藥物占31個、血液和造血系統(tǒng)藥物占18個。每批次的國采都能看到科倫藥業(yè)的身影,從最早的4+7試點一路走到第七批國采,總中標的產(chǎn)品數(shù)量為35個。
石藥集團歐意藥業(yè)的注射用紫杉醇(白蛋白結合型)4類仿制上市申請在2018年2月獲批并視同過評,成為了石藥控股首個過評的產(chǎn)品,截至2022年年底集團共有86個產(chǎn)品過評。過評產(chǎn)品分布在8個大類,其中全身用抗感染藥物占27個、神經(jīng)系統(tǒng)藥物、抗腫瘤和免疫調節(jié)劑、消化系統(tǒng)及代謝藥均超10個。石藥控股從聯(lián)盟擴圍階段開始參與國采,集團總中標產(chǎn)品數(shù)量為30個。
資料來源:米內網(wǎng)綜合數(shù)據(jù)庫注:米內網(wǎng)《中國公立醫(yī)療機構藥品終端競爭格局》,統(tǒng)計范圍是:中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院,不含民營醫(yī)院、私人診所、村衛(wèi)生室;上述銷售額以產(chǎn)品在終端的平均零售價計算。數(shù)據(jù)統(tǒng)計截至2022年12月31日,歡迎指正。

