9月22日訊 近日,揚(yáng)子江研發(fā)管線喜訊連連,1類新藥YZJ-2440馬來(lái)酸鹽片獲批臨床、3類仿制藥阿齊沙坦片報(bào)產(chǎn)......目前揚(yáng)子江有10款1類新藥在研,首個(gè)創(chuàng)新藥上市在即;63個(gè)以新分類報(bào)產(chǎn)品種在審,在2019年中國(guó)公立醫(yī)療機(jī)構(gòu)終端市場(chǎng)規(guī)模超過(guò)600億元;21個(gè)在審品種暫未有首仿獲批,11個(gè)品種由揚(yáng)子江首家或獨(dú)家以新分類報(bào)產(chǎn);35個(gè)品種順利過(guò)評(píng),比領(lǐng)跑的齊魯制藥僅少5個(gè)品種。
10款1類新藥在研,首個(gè)創(chuàng)新藥上市在即
9月11日,CDE官網(wǎng)顯示,揚(yáng)子江藥業(yè)自主研發(fā)的1類新藥YZJ-2440馬來(lái)酸鹽片獲得臨床試驗(yàn)?zāi)驹S可,擬用于治療HR+/HER2-晚期或轉(zhuǎn)移性乳腺癌。
米內(nèi)網(wǎng)數(shù)據(jù)顯示,目前揚(yáng)子江有2個(gè)1類新藥申報(bào)上市,2012年報(bào)產(chǎn)的艾拉莫德片于2016年被企業(yè)主動(dòng)撤回,目前未有新進(jìn)展,2019年報(bào)產(chǎn)的注射用磷酸左奧硝唑酯二鈉目前還處于“在審評(píng)審批中(在藥審中心)”;9個(gè)1類新藥已獲批臨床,最快研發(fā)進(jìn)展已完成II期臨床。
表1:揚(yáng)子江在研新藥

來(lái)源:米內(nèi)網(wǎng)中國(guó)藥品臨床試驗(yàn)公示庫(kù)
2019年8月,揚(yáng)子江藥業(yè)1類新藥注射用磷酸左奧硝唑酯二鈉上市申請(qǐng)獲得CDE承辦受理,用于治療婦科盆腔炎癥性疾病,同年11月以“具有明顯治療優(yōu)勢(shì)創(chuàng)新藥”為由納入優(yōu)先審評(píng)。該產(chǎn)品屬于硝基咪唑類抗生素,是奧硝唑左旋異構(gòu)體磷酸酯衍生物的鈉鹽,為已上市左奧硝唑的前藥。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年中國(guó)城市公立醫(yī)院、縣級(jí)公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡(jiǎn)稱中國(guó)公立醫(yī)療機(jī)構(gòu))終端奧硝唑及左奧硝唑銷售額分別突破30億元、2億元。
YZJ-1139片是食欲素1和2型雙重受體的高效拮抗劑,通過(guò)抑制食欲素受體從而改善睡眠,目前正在進(jìn)行II期臨床;鹽酸優(yōu)克那非片是一款PDE-5抑制劑,由吉林大學(xué)研發(fā),天士力申報(bào)臨床,揚(yáng)子江開展臨床研究,目前已完成治療勃起功能障礙的II期臨床,9月17日揚(yáng)子江提交該新藥補(bǔ)充申請(qǐng)獲得CDE承辦受理;YZJ-0673馬來(lái)酸鹽片是一種泛PI3K抑制劑,國(guó)內(nèi)尚無(wú)同靶點(diǎn)藥物獲批上市,揚(yáng)子江的產(chǎn)品正在進(jìn)行I期臨床,用于晚期惡性實(shí)體腫瘤;YZJ-0318馬來(lái)酸鹽片為第三代表皮生長(zhǎng)因子(EGFR-TKI)受體抑制劑,能夠選擇性的抑制T790M耐藥突變,目前正在開展I期臨床。
托西酸伊菲替尼片屬于替尼類小分子藥物,為特殊審評(píng)品種,注射用鹽酸頭孢他美為重大專項(xiàng)及特殊審評(píng)品種,YZJ-2440馬來(lái)酸鹽片、YZJ-1495鹽酸鹽膠囊均為2020年獲批臨床的新藥,作用靶點(diǎn)暫時(shí)未知。
63個(gè)新品緊盯600億市場(chǎng),21個(gè)品種搶首仿
揚(yáng)子江藥業(yè)在仿制藥的研發(fā)也收獲頗豐,2020年至今已有11個(gè)新品獲批上市,均以新注冊(cè)分類報(bào)產(chǎn),獲批生產(chǎn)后視同通過(guò)一致性評(píng)價(jià);23個(gè)新品申請(qǐng)上市(含新規(guī)格報(bào)產(chǎn)),注冊(cè)分類為仿制3類或仿制4類。
表2:揚(yáng)子江新分類報(bào)產(chǎn)在審品種


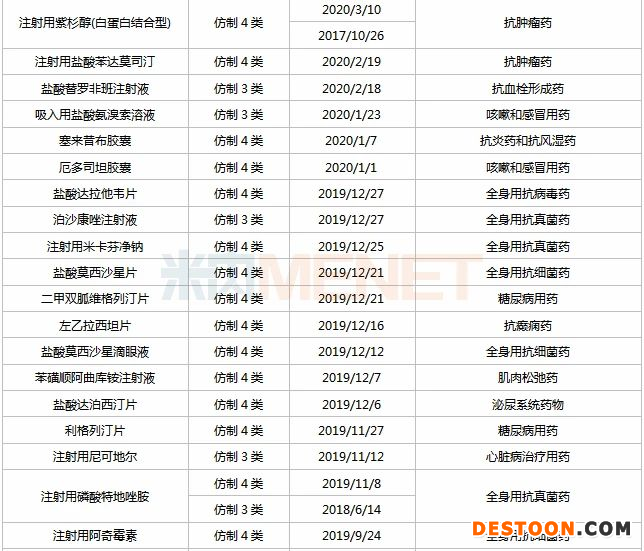


來(lái)源:米內(nèi)網(wǎng)MED2.0中國(guó)藥品審評(píng)數(shù)據(jù)庫(kù)
截至9月18日,揚(yáng)子江有77個(gè)品種以新注冊(cè)分類報(bào)產(chǎn),14個(gè)已獲批生產(chǎn)并視同通過(guò)一致性評(píng)價(jià),在審的63個(gè)品種在2019年中國(guó)公立醫(yī)療機(jī)構(gòu)終端合計(jì)市場(chǎng)規(guī)模超過(guò)600億元,其中有21個(gè)品種超過(guò)10億元。
從治療類別看,全身用抗感染藥物、神經(jīng)系統(tǒng)藥物是揚(yáng)子江主攻的兩大用藥領(lǐng)域,分別有18個(gè)、10個(gè)品種在審,米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年中國(guó)公立醫(yī)療機(jī)構(gòu)終端全身用抗感染藥物、神經(jīng)系統(tǒng)藥物市場(chǎng)規(guī)模分別突破2000億元、1000億元。
表3:未有仿制藥獲批上市的品種


來(lái)源:米內(nèi)網(wǎng)MED2.0中國(guó)藥品審評(píng)數(shù)據(jù)庫(kù)
揚(yáng)子江在審的63個(gè)品種中有21個(gè)在國(guó)內(nèi)市場(chǎng)暫未有首仿(含劑型首仿)獲批上市。全球銷售額較高的品種有泊馬度胺膠囊,該產(chǎn)品具有多種作用機(jī)制,是多發(fā)性骨髓瘤治療領(lǐng)域的重磅免疫調(diào)節(jié)劑,2019年全球銷售額達(dá)25.25億美元,原研還未獲批進(jìn)口,正大天晴、揚(yáng)子江、齊魯3家企業(yè)以新分類報(bào)產(chǎn);舒更葡糖鈉注射液是全球首個(gè)用于逆轉(zhuǎn)神經(jīng)肌肉阻滯劑的選擇性松弛拮抗劑,2019年全球銷售額達(dá)11.31億美元,原研已獲批進(jìn)口,科倫、揚(yáng)子江、東陽(yáng)光藥、齊魯?shù)?2家企業(yè)搶首仿。
11個(gè)品種由揚(yáng)子江首家或獨(dú)家以新分類報(bào)產(chǎn),獲得首仿的幾率比較大。其中氫溴酸伏硫西汀片、鹽酸右美托咪定氯化鈉注射液、恩替卡韋口服液3個(gè)品種由揚(yáng)子江首家以新分類報(bào)產(chǎn);注射用磷酸特地唑胺、鹽酸達(dá)拉他韋片、富馬酸盧帕他定口服液、鹽酸奈康唑乳膏、甲磺酸沙芬酰胺片、復(fù)方電解質(zhì)注射液(Ⅲ)、醋酸鈉林格葡萄糖注射液、硫酸鈉鉀鎂口服溶液8個(gè)品種由揚(yáng)子江獨(dú)家以新分類報(bào)產(chǎn)。
13個(gè)為首家,35個(gè)過(guò)評(píng)品種趕追齊魯
在一致性評(píng)價(jià)方面,2020年至今,揚(yáng)子江有17個(gè)品種通過(guò)或視同通過(guò)一致性評(píng)價(jià)(含新品規(guī)過(guò)評(píng)),其中11個(gè)品種以新分類報(bào)產(chǎn)而視同過(guò)評(píng),6個(gè)品種提交補(bǔ)充申請(qǐng)而過(guò)評(píng)。
表4:揚(yáng)子江已過(guò)評(píng)品種


來(lái)源:米內(nèi)網(wǎng)MED2.0中國(guó)藥品審評(píng)數(shù)據(jù)庫(kù)
截至9月18日,341個(gè)品種已有企業(yè)通過(guò)或視同通過(guò)一致性評(píng)價(jià),從企業(yè)過(guò)評(píng)情況看,齊魯制藥以40個(gè)過(guò)評(píng)品種領(lǐng)跑,中國(guó)生物制藥以36個(gè)品種緊接其后,揚(yáng)子江藥業(yè)以35個(gè)品種排位第三。揚(yáng)子江過(guò)評(píng)品種中,有13個(gè)品種為首家過(guò)評(píng),其中頭孢丙烯片、依帕司他片、鹽酸特拉唑嗪膠囊、枸櫞酸他莫昔芬片4個(gè)品種為獨(dú)家過(guò)評(píng)。
在日前開展的第三批國(guó)家集采中,揚(yáng)子江有7個(gè)品種成功中標(biāo),分別為阿那曲唑片(4家中標(biāo))、非那雄胺片(1mg,2家中標(biāo))、孟魯司特鈉咀嚼片(6家中標(biāo))、替格瑞洛片(6家中標(biāo))、維格列汀片(6家中標(biāo))、鹽酸西替利嗪片(5家中標(biāo))、左氧氟沙星滴眼液(2家中標(biāo))。在2019年中國(guó)公立醫(yī)療機(jī)構(gòu)終端競(jìng)爭(zhēng)格局中,揚(yáng)子江在這7大品種所占市場(chǎng)份額均較低或?yàn)?,如今順利中標(biāo),可借此迅速搶占市場(chǎng)。
注:數(shù)據(jù)統(tǒng)計(jì)截至9月18日,如有疏漏,歡迎指正!



 110102000668(1)號(hào)
110102000668(1)號(hào)