6月30日,奧賽康發(fā)布公告稱,全資子公司江蘇奧賽康藥業(yè)于近日收到國家藥監(jiān)局下發(fā)的艾曲泊帕乙醇胺片的上市申請《受理通知書》。據(jù)悉,艾曲泊帕乙醇胺片是諾華公司開發(fā)的一種非肽類血小板生成素受體激動(dòng)劑,2019年全球銷售額超過14億美元。目前,江蘇奧賽康藥業(yè)是該產(chǎn)品國內(nèi)第一家完成BE并遞交生產(chǎn)注冊申請的企業(yè)。
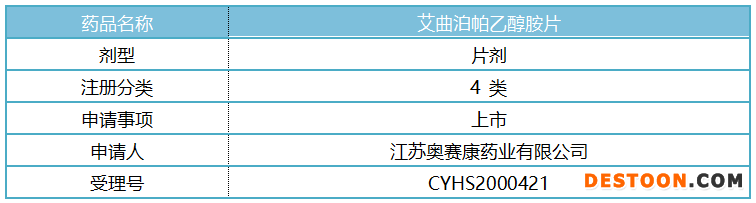


表1:藥品基本情況

來源:公司公告
圖1:艾曲泊帕的全球銷售情況(單位:百萬美元)

來源:米內(nèi)網(wǎng)跨國上市公司銷售數(shù)據(jù)庫
據(jù)悉,艾曲泊帕乙醇胺片是諾華公司開發(fā)的一種非肽類血小板生成素受體激動(dòng)劑,2008年11月獲得FDA批準(zhǔn)上市,用于治療既往對糖皮質(zhì)激素、免疫球蛋白等治療反應(yīng)不佳的慢性免疫性(特發(fā)性)血小板減少癥(ITP)。它是首個(gè)治療ITP的口服藥物,給藥更加方便,患者依從性高,明顯降低出血率,維持ITP患者的血小板計(jì)數(shù),減少輸血。美國批準(zhǔn)的適應(yīng)癥范圍更廣泛,除用于ITP成人,還批準(zhǔn)用于一歲以上患兒。
米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年艾曲泊帕全球銷售額超過14億美元。原研艾曲泊帕乙醇胺片于2017年12月獲批進(jìn)入中國,商品名為瑞弗蘭,2019年在中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端銷售額超過1800萬元。
圖2:艾曲泊帕乙醇胺片國內(nèi)上市申請情況

來源:米內(nèi)網(wǎng)一鍵檢索
公告中提到,江蘇奧賽康藥業(yè)是該產(chǎn)品國內(nèi)第一家完成了臨床生物等效性研究遞交生產(chǎn)注冊申請的企業(yè),米內(nèi)網(wǎng)數(shù)據(jù)顯示,奧賽康分別在2020年1月及6月申報(bào)過艾曲泊帕乙醇胺片的4類仿制上市申請,目前兩個(gè)受理號均在審評審批中。
來源:米內(nèi)網(wǎng)數(shù)據(jù)庫、公司公告
審評數(shù)據(jù)統(tǒng)計(jì)截至2020年7月1日,如有錯(cuò)漏,敬請指正。



 110102000668(1)號
110102000668(1)號