11月6日訊 11月5日,CDE官網(wǎng)顯示,四川匯宇制藥以仿制4類提交的左乙拉西坦注射用濃溶液上市申請(qǐng)獲得CDE承辦受理。2020年至今,四川匯宇制藥已有5個(gè)品種(均為注射劑)以新分類報(bào)產(chǎn),其中普樂(lè)沙福注射液暫無(wú)首仿,四川匯宇制藥獨(dú)家以新分類報(bào)產(chǎn)。
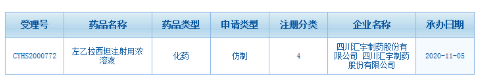
來(lái)源:CDE官網(wǎng)
左乙拉西坦是一種吡咯烷酮衍生物,適用于成人及4歲以上兒童癲癇患者部分性發(fā)作(伴或不伴繼發(fā)性全面性發(fā)作)的加用治療。該產(chǎn)品由比利時(shí)公司研發(fā),主要?jiǎng)┬桶ㄆ瑒?、溶液劑及注射劑,其中注射劑型?006年7月獲得FDA批準(zhǔn)上市,2017年7月獲批進(jìn)入國(guó)內(nèi)市場(chǎng)。
米內(nèi)網(wǎng)數(shù)據(jù)顯示,近幾年來(lái)左乙拉西坦在中國(guó)城市公立醫(yī)院、縣級(jí)公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡(jiǎn)稱中國(guó)公立醫(yī)療機(jī)構(gòu))終端銷售額逐年上漲,2019年超過(guò)10億元,同比增長(zhǎng)12.54%。左乙拉西坦注射用濃溶液在國(guó)內(nèi)上市時(shí)間較晚,尚未形成規(guī)模銷售,2019年占左乙拉西坦總體市場(chǎng)比重為2.1%,2020年H1上升至4.2%。
圖:左乙拉西坦注射用濃溶液過(guò)評(píng)情況

來(lái)源:米內(nèi)網(wǎng)一致性評(píng)價(jià)數(shù)據(jù)庫(kù)
目前已有5家企業(yè)的左乙拉西坦注射用濃溶液視同通過(guò)一致性評(píng)價(jià),分別為河北仁合益康藥業(yè)、濟(jì)川藥業(yè)、重慶圣華曦藥業(yè)、海南普利制藥及江蘇萬(wàn)高藥業(yè),其中河北仁合益康藥業(yè)為首家過(guò)評(píng)。
表:2020年至今四川匯宇制藥新分類報(bào)產(chǎn)品種
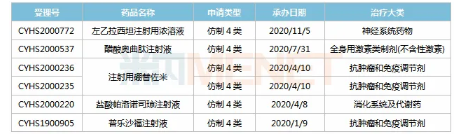
來(lái)源:米內(nèi)網(wǎng)MED2.0中國(guó)藥品審評(píng)數(shù)據(jù)庫(kù)
米內(nèi)網(wǎng)數(shù)據(jù)顯示,2020年至今,四川匯宇制藥已有5個(gè)品種以新分類報(bào)產(chǎn),均為注射劑。普樂(lè)沙福注射液暫未有仿制藥獲批上市,目前由四川匯宇制藥獨(dú)家以新分類報(bào)產(chǎn)。
來(lái)源:米內(nèi)網(wǎng)數(shù)據(jù)庫(kù)、CDE官網(wǎng)



 110102000668(1)號(hào)
110102000668(1)號(hào)