11月9日訊 注射劑一致性評(píng)價(jià)扎堆,集采沖擊6000億市場(chǎng)
沉寂兩年有余,注射劑一致性評(píng)價(jià)補(bǔ)充申請(qǐng)大開閘,正大天晴、健康元、海普瑞……注射劑紛紛拿下首家過評(píng)。目前已有51款注射劑(108個(gè)品規(guī))通過/視同通過一致性評(píng)價(jià),正大、恒瑞、齊魯?shù)绕髽I(yè)領(lǐng)跑過評(píng)榜。今年以來,國(guó)家層面在注射劑一致性評(píng)價(jià)領(lǐng)域動(dòng)作頻頻,NMPA、CDE相繼出臺(tái)相關(guān)文件、國(guó)采計(jì)劃提高注射劑比重等。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2020H1中國(guó)公立醫(yī)療機(jī)構(gòu)終端化藥注射劑銷售額為2632億元,同比下滑15.15%。第四批集采已是如箭在弦,注射劑降價(jià)潮將加速到來。
注射劑一致性評(píng)價(jià)開閘!齊魯、豪森、正大天晴……扎堆過評(píng)
沉寂兩年有余,注射劑一致性評(píng)價(jià)大開閘,多款注射劑相繼通過一致性評(píng)價(jià)補(bǔ)充申請(qǐng)。這也意味著,注射劑國(guó)采的大網(wǎng)即將鋪開。
通過一致性評(píng)價(jià)補(bǔ)充申請(qǐng)的注射劑
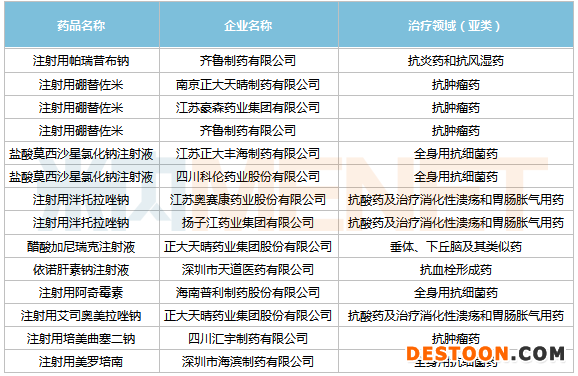
來源:米內(nèi)網(wǎng)MED2.0中國(guó)藥品審評(píng)數(shù)據(jù)庫
10月12日,海普瑞孫公司天道醫(yī)藥的依諾肝素鈉注射液(5個(gè)規(guī)格)通過一致性評(píng)價(jià),海普瑞為國(guó)內(nèi)肝素原料藥龍頭,公司的依諾肝素鈉注射液為肝素大市場(chǎng)首個(gè)過評(píng)品種。緊接著,5款注射劑首家過評(píng)企業(yè)也接連誕生,分別為健康元子公司海濱制藥的注射用美羅培南、正大天晴藥業(yè)集團(tuán)的醋酸加尼瑞克注射液及注射用艾司奧美拉唑鈉、奧賽康的注射用泮托拉唑鈉、青峰藥業(yè)的拉考沙胺注射液。
此外,齊魯制藥的注射用帕瑞昔布鈉及注射用硼替佐米、科倫藥業(yè)和正大豐海的鹽酸莫西沙星氯化鈉注射液、南京正大天晴和豪森藥業(yè)的注射用硼替佐米也紛紛過評(píng)。目前,這3款注射劑的過評(píng)企業(yè)均達(dá)到4家。而鹽酸莫西沙星氯化鈉注射液已納入第三批集采,注射用帕瑞昔布鈉、注射用硼替佐米無疑是第四批集采的“獵物”。
距離上一次注射劑通過補(bǔ)充申請(qǐng),已經(jīng)有兩年多的時(shí)間。2018年5月,普利制藥的注射用阿奇霉素成為首個(gè)通過一致性評(píng)價(jià)補(bǔ)充申請(qǐng)的注射劑;2018年6月,匯宇制藥以仿制4類獲批的注射用培美曲塞二鈉通過補(bǔ)充申請(qǐng)。
51款注射劑過評(píng)!正大天晴、恒瑞、齊魯……領(lǐng)跑
通過/視同通過一致性評(píng)價(jià)的注射劑
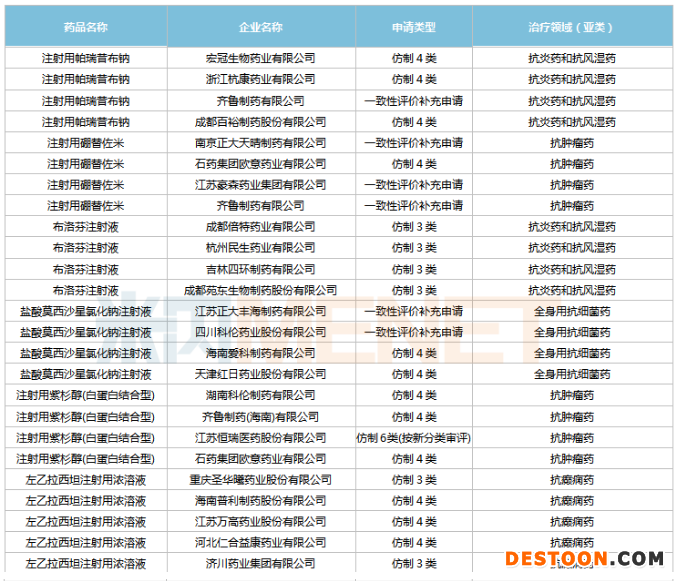
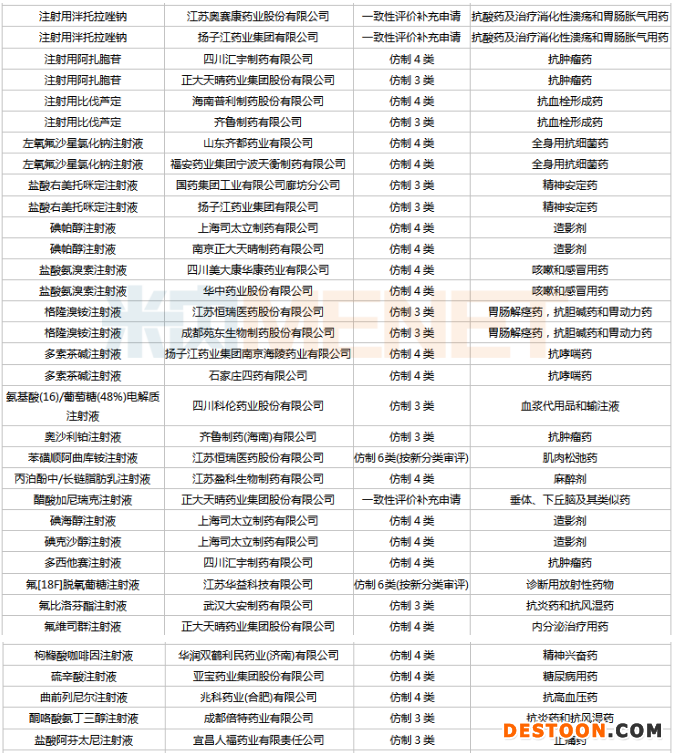
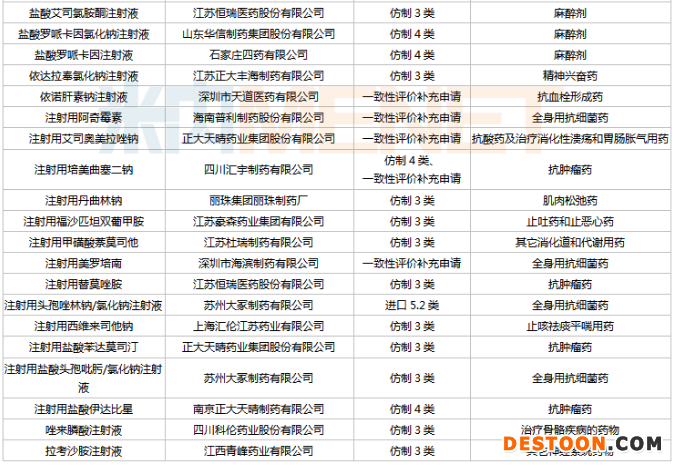
來源:米內(nèi)網(wǎng)MED2.0中國(guó)藥品審評(píng)數(shù)據(jù)庫
米內(nèi)網(wǎng)一致性評(píng)價(jià)數(shù)據(jù)庫顯示,截至目前已有51款注射劑(108個(gè)品規(guī))通過/視同通過一致性評(píng)價(jià)。中國(guó)生物制藥(正大天晴、正大豐海)以10個(gè)注射劑品種領(lǐng)跑,其附屬公司正大天晴藥業(yè)集團(tuán)、南京正大天晴、正大豐海分別有5、3、2款注射劑過評(píng)。
此外,恒瑞醫(yī)藥、齊魯制藥均有5款注射劑過評(píng),科倫藥業(yè)則有4款注射劑過評(píng),揚(yáng)子江藥業(yè)集團(tuán)、匯宇制藥、司太立、普利制藥等4家企業(yè)均有3個(gè)注射劑品種過評(píng)。在注射劑一致性評(píng)價(jià)補(bǔ)充申請(qǐng)與新注冊(cè)分類雙通道并行的情況,后續(xù)還會(huì)有更多企業(yè)的產(chǎn)品過評(píng),但中國(guó)生物制藥已是遙遙領(lǐng)先。
從品種過評(píng)情況看,注射用紫杉醇(白蛋白結(jié)合型)、布洛芬注射液、左乙拉西坦注射用濃溶液、鹽酸莫西沙星氯化鈉注射液、注射用硼替佐米、注射用帕瑞昔布鈉等6款注射劑過評(píng)企業(yè)已經(jīng)超過3家。其中,僅布洛芬注射液、注射用硼替佐米、注射用帕瑞昔布鈉等3款注射劑尚未國(guó)采,大概率進(jìn)入第四批國(guó)采目錄。
鹽酸右美托咪定注射液、注射用阿扎胞苷、鹽酸氨溴索注射液、多索茶堿注射液、碘帕醇注射液、左氧氟沙星氯化鈉注射液、注射用泮托拉唑鈉、注射用比伐蘆定、格隆溴銨注射液等9款注射劑過評(píng)企業(yè)均有2家,其余注射劑均為獨(dú)家過評(píng)。
在國(guó)家開展的三批集采中,注射劑共有7個(gè)品種被納入,分別為氟比洛芬酯注射液、注射用培美曲塞二鈉、鹽酸右美托咪定注射液、注射用紫杉醇(白蛋白結(jié)合型)、注射用阿扎胞苷、左乙拉西坦注射用濃溶液、鹽酸莫西沙星氯化鈉注射液。其中,氟比洛芬酯注射液、注射用培美曲塞二鈉目前仍只有一家企業(yè)過評(píng)。
第四批國(guó)采將來襲!注射劑被“盯上”
米內(nèi)網(wǎng)MED2.0中國(guó)藥品審評(píng)數(shù)據(jù)庫顯示,截至11月5日,注射劑一致性評(píng)價(jià)申請(qǐng)?jiān)趯徳u(píng)品種有181個(gè)(涉及907個(gè)品規(guī)),新注冊(cè)分類(仿制3類、4類)在審評(píng)品種有219個(gè)(涉及593個(gè)品規(guī))。
2020年5月14日,國(guó)家藥監(jiān)局發(fā)布《關(guān)于開展化學(xué)藥品注射劑仿制藥質(zhì)量和療效一致性評(píng)價(jià)工作的公告》,標(biāo)志著化藥注射劑一致性評(píng)價(jià)工作正式啟動(dòng)。10月21日,CDE發(fā)布《關(guān)于注射劑一致性評(píng)價(jià)補(bǔ)充資料相關(guān)事宜的通知》,為提高注射劑一致性評(píng)價(jià)工作效率、優(yōu)化審評(píng)審批流程,對(duì)企業(yè)注冊(cè)申報(bào)資料的合規(guī)性完整性提出更高要求,補(bǔ)充資料遲交、有實(shí)質(zhì)性缺陷將不批準(zhǔn)。這意味著,注射劑品種過評(píng)數(shù)量將大幅提升。
實(shí)際上,這一切都是為第四批集采做鋪墊。2020年9月,一則關(guān)于國(guó)家藥品集采的相關(guān)談話在業(yè)內(nèi)流傳。內(nèi)容包括:國(guó)家集采將常態(tài)化開展,只要符合集采條件的品種數(shù)或其金額達(dá)到一定水平,即觸發(fā)啟動(dòng)國(guó)家集采,預(yù)計(jì)每年開展兩批;明年開始將逐步提高注射劑在國(guó)家集采中的比重。
中國(guó)公立醫(yī)療機(jī)構(gòu)終端化藥注射劑銷售情況
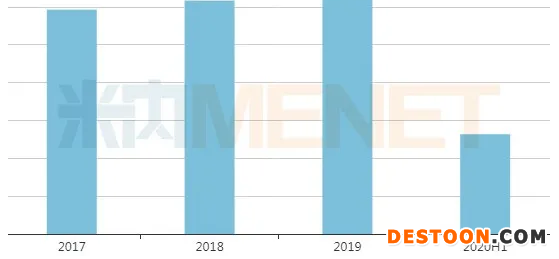
來源:米內(nèi)網(wǎng)中國(guó)公立醫(yī)療機(jī)構(gòu)終端競(jìng)爭(zhēng)格局
米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年中國(guó)城市公立醫(yī)院、縣級(jí)公立醫(yī)院、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡(jiǎn)稱中國(guó)公立醫(yī)療機(jī)構(gòu))終端化藥注射劑銷售額為6369億元;2020H1其銷售額為2632億元,同比下滑15.15%。隨著注射劑一致性評(píng)價(jià)審評(píng)審批提速,過評(píng)品種納入國(guó)采的時(shí)間將縮短,未過評(píng)品種則成為地方省采考慮對(duì)象,注射劑降價(jià)潮將加速到來。
來源:米內(nèi)網(wǎng)數(shù)據(jù)庫
審評(píng)數(shù)據(jù)統(tǒng)計(jì)截至2020年11月5日,如有疏漏,歡迎指正!



 110102000668(1)號(hào)
110102000668(1)號(hào)