近日,2023國談再傳新消息,調整重點繼續(xù)向兒童藥、罕見病藥等方面傾斜。據統(tǒng)計,國家醫(yī)保已納入至少60個罕見病藥,其中不乏人免疫球蛋白、瑞舒伐他汀等2022年在中國公立醫(yī)療機構終端銷售規(guī)模超5億元的大品種,以及諾西那生鈉、尼達尼布等銷售增速超三位數(shù)的潛力明星藥。7月已至,新一輪國談已進入申報階段,40個罕見病藥蓄勢待發(fā),最終醫(yī)保準入情況如何,11月有望見分曉。
在臨床用藥需求推動下,罕見病藥物市場持續(xù)升溫。有業(yè)內專業(yè)機構指出,中國罕見病藥市場于2016年及2020年分別占全球罕見病市場的0.4%及1%,預計2030年將激增至259億美元,約合1755億元(按實時匯率換算)。
為進一步滿足罕見病藥市場的快速增長,鼓勵藥企加大對罕見病藥的研發(fā)和生產,近年來,國家相繼出臺了一系列鼓勵政策,如《第一批罕見病目錄》的發(fā)布,共涉及121種罕見病,為各部門制定罕見病相關政策提供重要依據;《關于加大對罕見病診治投入力度的建議》答復中指出,將積極推進成立國家級權威罕見病學術組織,適時調整更新第二批罕見病目錄……
01、60個品種納入醫(yī)保 第一批罕見病目錄覆蓋率僅22%
政策落地全面驅動研發(fā),但從罕見病藥獲批及“進保”情況來看并不理想。
數(shù)據顯示,2009版國家醫(yī)保目錄包含22個罕見病藥,覆蓋13個罕見??;2017版國家醫(yī)保目錄包含30個罕見病藥,覆蓋15個罕見病;2019版國家醫(yī)保目錄包含39個罕見病藥,覆蓋19個罕見??;2020版國家醫(yī)保目錄包含45個罕見病藥,覆蓋23個罕見??;2021版國家醫(yī)保目錄包含53個罕見病藥,覆蓋26個罕見?。?022版國家醫(yī)保目錄包含60個罕見病藥,覆蓋27個罕見病。
2018年6月,國家衛(wèi)健委公布《國家第一批罕見病目錄》,涉及121個病種;目前有醫(yī)保覆蓋的罕見病僅27個,覆蓋率僅為兩成。
已納入醫(yī)保目錄的罕見病藥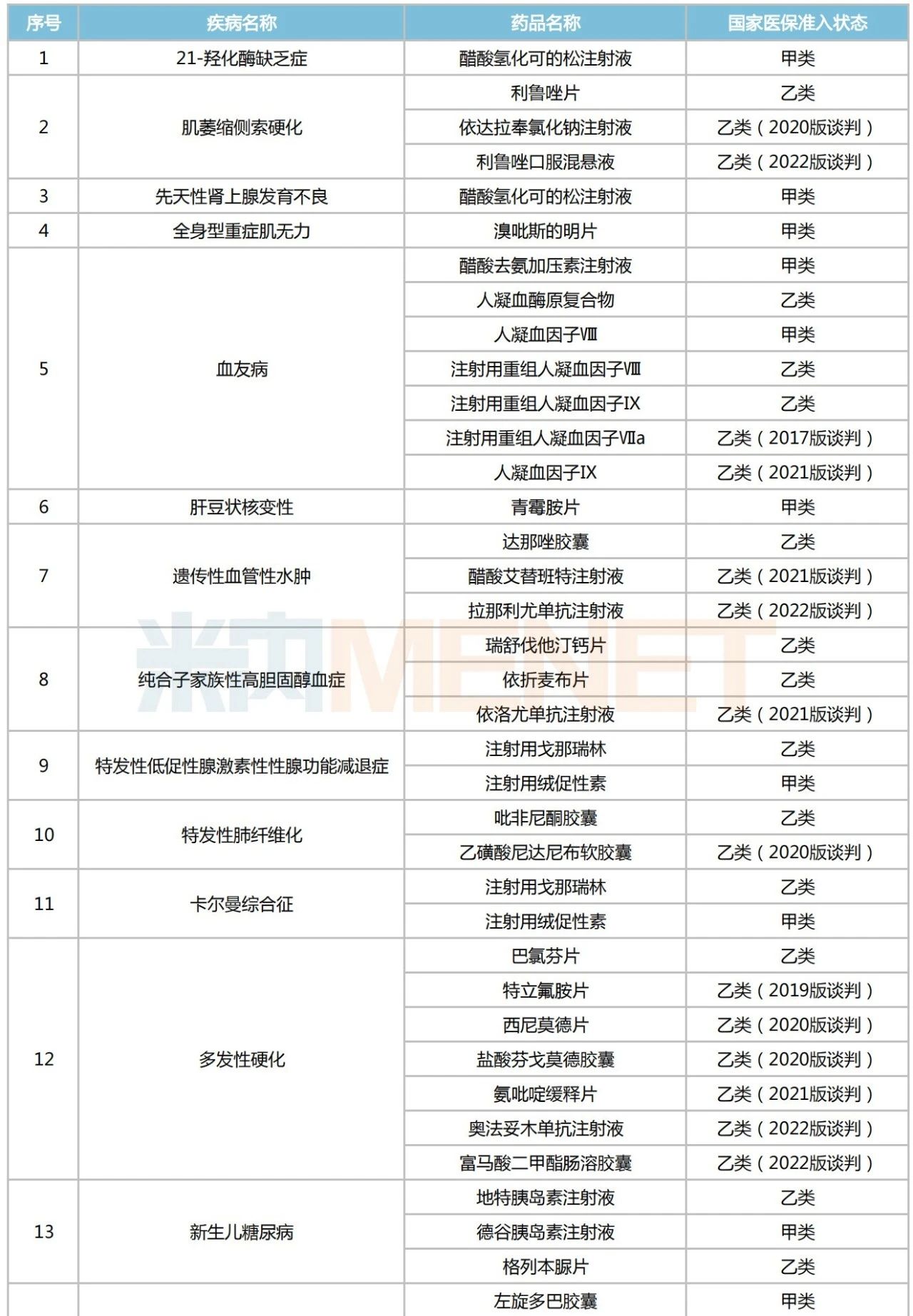

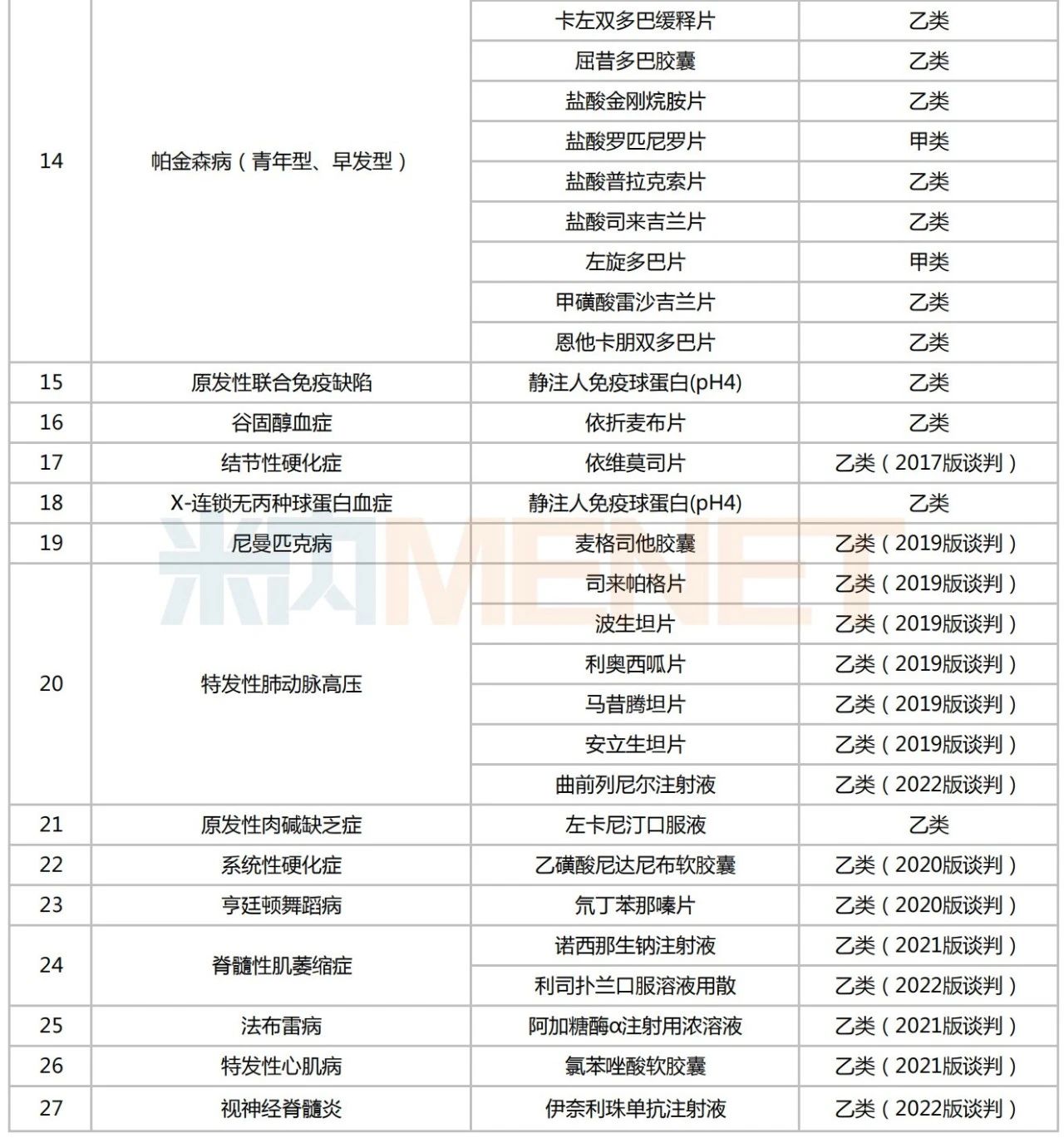
60個納入國家醫(yī)保的罕見病藥中,以帕金森病(青年型、早發(fā)型)、血友病、多發(fā)性硬化和特發(fā)性肺動脈高壓等病種居多,都在6個及以上。
結合近年來獲批的新藥及其進入醫(yī)保情況來看,目前上市的罕見病藥對應的適應癥還未能完全覆蓋第一批罕見病目錄的適應癥,臨床需求仍有未滿足的空間。
02、8大品種銷售額破5億 科倫、石藥.....潛力明星藥迎暴漲
數(shù)據顯示,60個罕見病藥中有8個在2022年中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機構)終端銷售額超過5億元,包括靜注人免疫球蛋白(pH4)、瑞舒伐他汀鈣片、注射用重組人凝血因子Ⅷ、依折麥布片、德谷胰島素注射液、人凝血因子Ⅷ、地特胰島素注射液、以及諾西那生鈉注射液。
然而,罕見病并非上述產品的主要適應癥,像靜注人免疫球蛋白(pH4)屬于全身用抗感染藥物,主要用于預防麻疹和傳染性肝炎,以及與抗生素聯(lián)用,提高對某些嚴重細菌和病毒感染的療效;瑞舒伐他汀鈣片、依折麥布片均是經典降血脂藥;注射用重組人凝血因子Ⅷ最初用作急診或擇期手術中的止血劑;德谷胰島素注射液、地特胰島素注射液則是臨床常用的胰島素降糖藥。
8個銷售額突破5億的罕見病藥(單位:億元)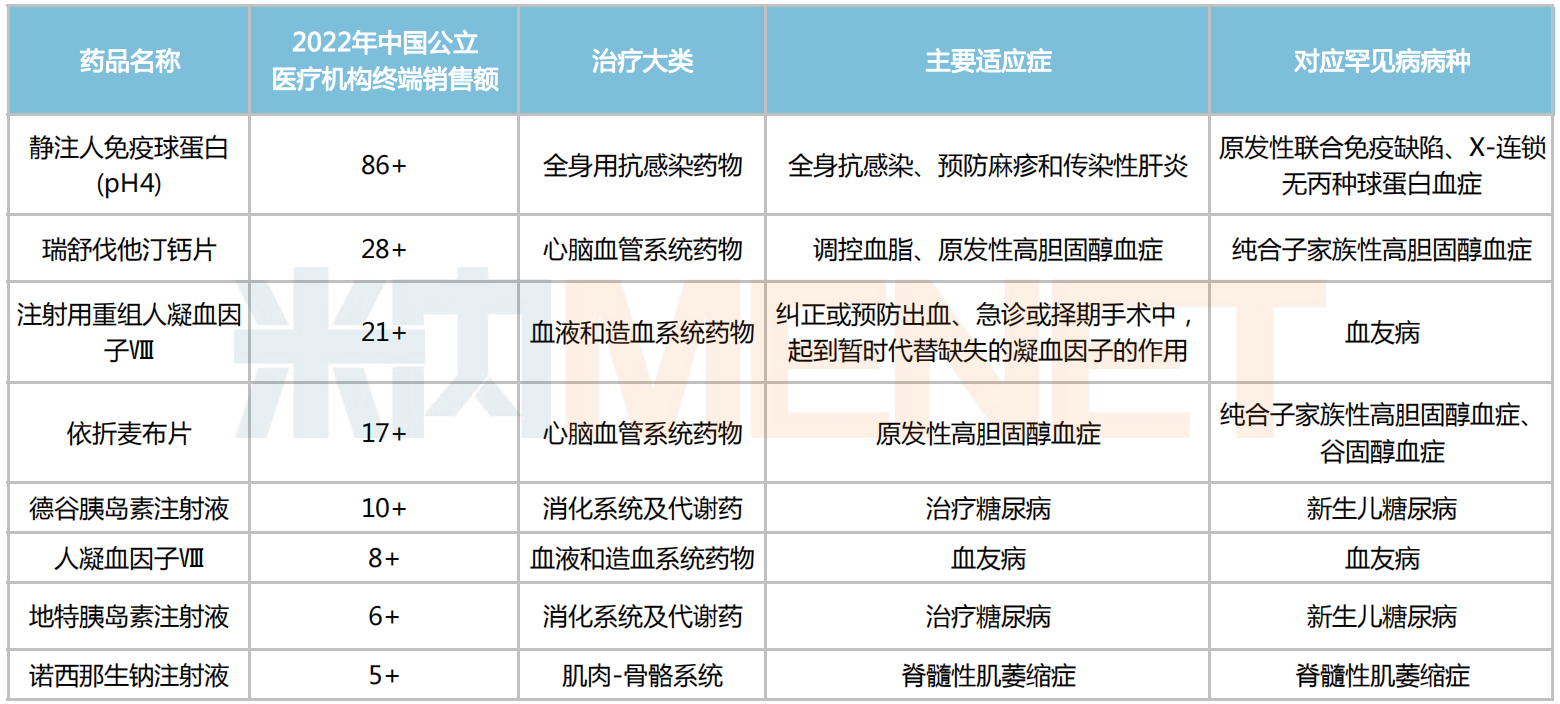

目前來看,大部分的罕見病藥市場規(guī)模仍然較小,一方面可能是因為藥品剛上市,尚未實現(xiàn)放量;另一方面也可能因為市場所監(jiān)測的醫(yī)院不是用藥的主要醫(yī)院。不過,仍有部分以罕見病為主要適應癥的品種市場潛力不容小覷。
7個銷售額增速超三位數(shù)的罕見病藥
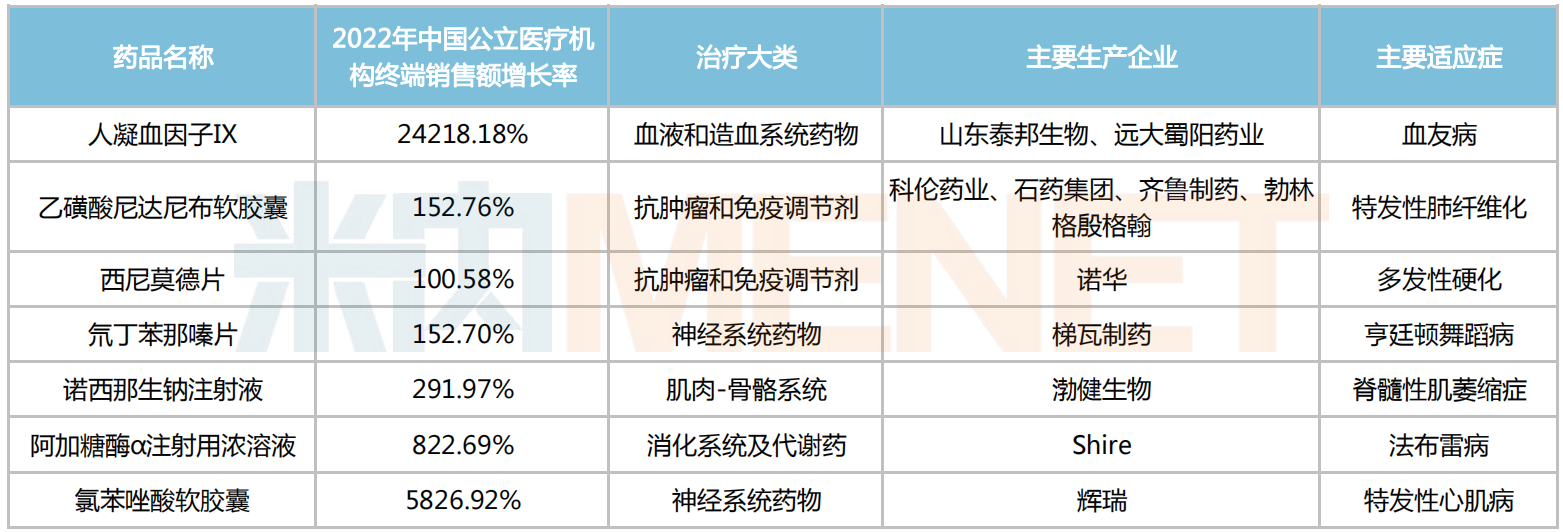
數(shù)據顯示,7個罕見病藥2022年在中國公立醫(yī)療機構終端銷售額增速超過三位數(shù)。其中,治療脊髓性肌萎縮癥的諾西那生鈉注射液,通過談判后降價95%進入醫(yī)保,2022年銷售額接近6億元,同比增長291.97%,增速十分驚人。
近年來中國公立醫(yī)療機構終端諾西那生鈉注射液銷售趨勢(單位:萬元)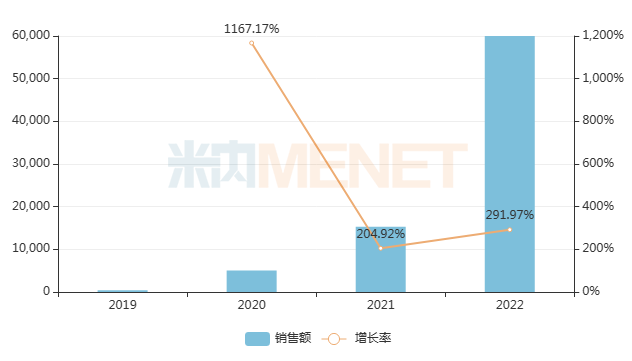

用于特發(fā)性肺纖維化的乙磺酸尼達尼布軟膠囊,目前已有勃林格殷格翰、科倫藥業(yè)、石藥集團、齊魯制藥4家企業(yè)獲批生產。自2020年通過談判納入醫(yī)保后,該藥市場規(guī)??焖贁U容。在中國公立醫(yī)療機構終端,乙磺酸尼達尼布軟膠囊2020、2021、2022年銷售額分別同比增長927%、2906%和152%,市場潛力在釋放。
近年來中國公立醫(yī)療機構終端乙磺酸尼達尼布軟膠囊銷售趨勢(單位:萬元)

總體而言,罕見病藥降價進入醫(yī)保只是過程,加速產品放量、提高患者的用藥可及性才是企業(yè)的最終目的和使命。
03、2023年國談在路上40個罕見病藥蓄勢待發(fā)
“讓更多罕見病藥盡快納入醫(yī)保”,國家也是不留余力。
近日,國家醫(yī)保局發(fā)布的“2023版國家醫(yī)保目錄調整工作方案”(下文簡稱調整方案)中指出,新一輪國談重點繼續(xù)向兒童藥、罕見病藥等傾斜:納入鼓勵仿制藥品目錄或鼓勵研發(fā)申報兒童用藥清單的藥品,以及罕見病治療藥,且于2023年6月30日前獲NMPA批準上市的均可申報。
據不完全統(tǒng)計,目前至少有40款罕見病藥有望參與2023年國談,其中用于黏多糖貯積癥、戈謝病及多發(fā)性硬化等罕見病的治療藥較多;劑型上以注射劑、片劑為主;從治療大類看,消化系統(tǒng)及代謝藥、抗腫瘤和免疫調節(jié)劑、以及神經系統(tǒng)藥物分別占據9個及以上的席位。
部分有機會參與2023年國談的罕見病藥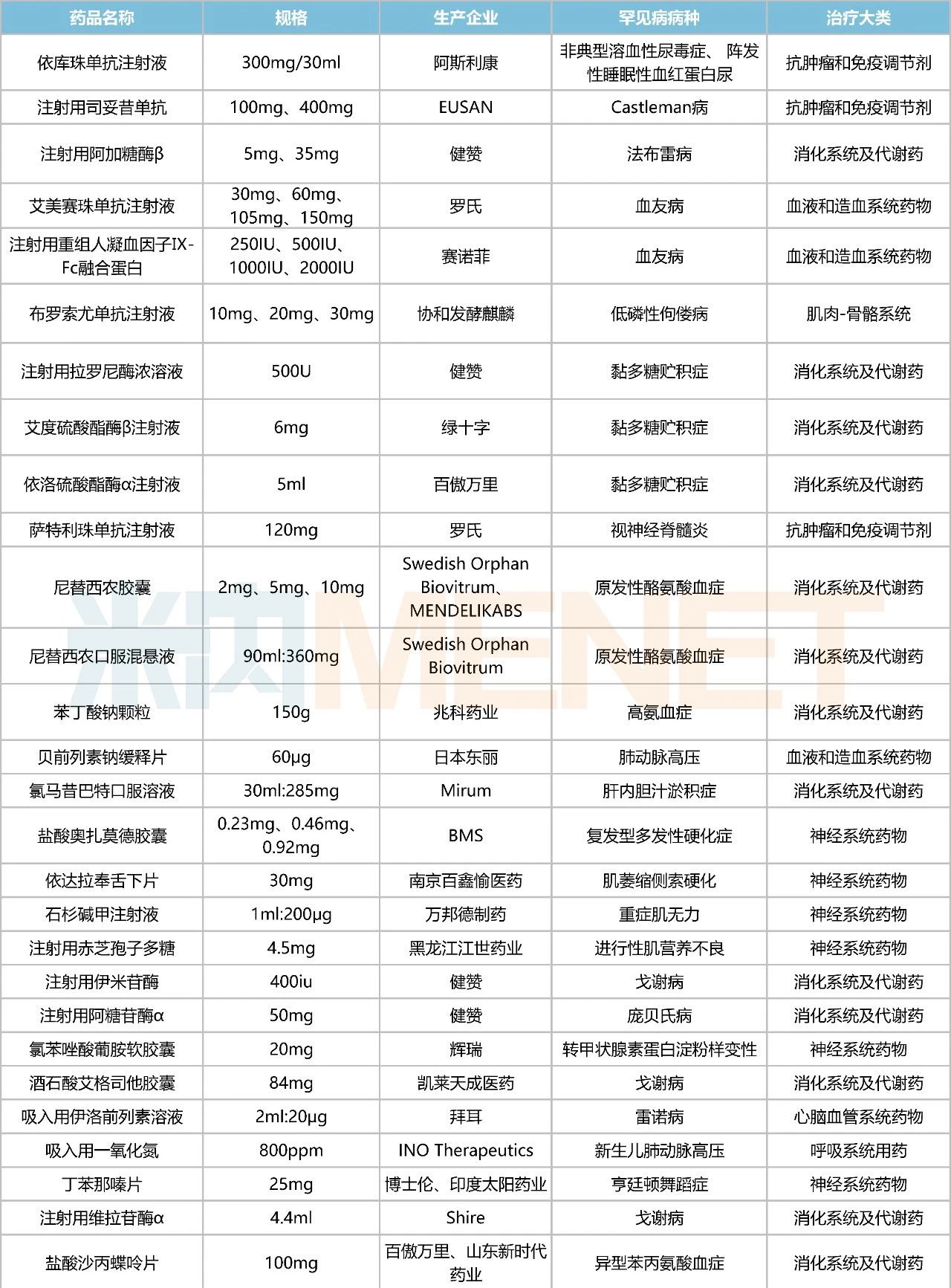

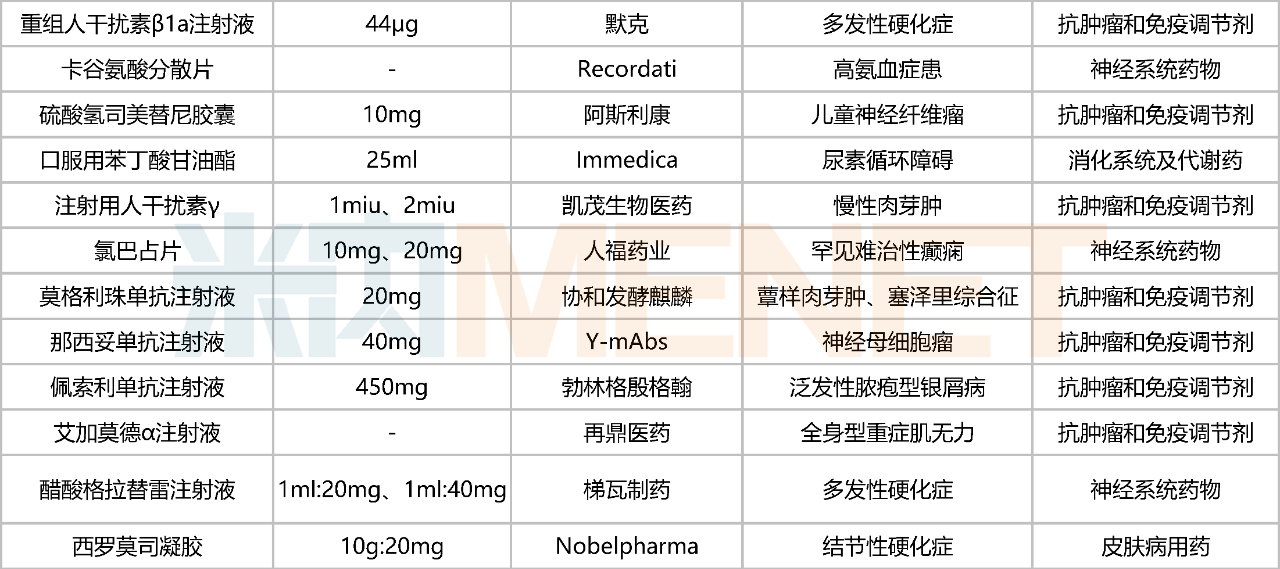
值得一提的是,多款罕見病藥“踩點”趕進考場(2023年6月30日前獲批),包括再鼎醫(yī)藥的艾加莫德α注射液(進口3.1類)、Recordati的卡谷氨酸分散片(進口5.1類)、梯瓦制藥的醋酸格拉替雷注射液(進口5.1類)、山東新時代藥業(yè)的鹽酸沙丙蝶呤片(仿制4類)、Immedica的口服用苯丁酸甘油酯(進口5.1類)、Mirum的氯馬昔巴特口服溶液(進口1類)、阿斯利康的依庫珠單抗注射液(進口3.1類:重癥肌無力)等罕見病藥均在今年6月獲NMPA批準。
驕陽似火,七月已至。根據調整方案的工作安排(5-6月:準備階段;7-8月:申報階段;8-9月:專家審評階段;9-11月:談判/競價階段;11月:醫(yī)保目錄公布),2023年國談已進入申報階段。屆時,哪些品種能成功入選,我們拭目以待!
來源:米內網數(shù)據庫、國家醫(yī)保局官網等;數(shù)據統(tǒng)計截至7月7日,如有疏漏,歡迎指正!

