12月1日訊 11月28日,CDE官網(wǎng)數(shù)據(jù)顯示,齊魯制藥申報(bào)的溴莫尼定噻嗎洛爾滴眼液4類仿制上市申請獲得受理。該產(chǎn)品適用于降低開角型青光眼及高眼壓癥患者的眼內(nèi)壓,目前國內(nèi)市場僅有美國艾爾建獲批進(jìn)口,齊魯制藥為該產(chǎn)品首家申報(bào)仿制上市的藥企。
圖1:齊魯制藥申報(bào)的溴莫尼定噻嗎洛爾滴眼液

來源:CDE官網(wǎng)
圖2:眼科用藥的市場規(guī)模情況
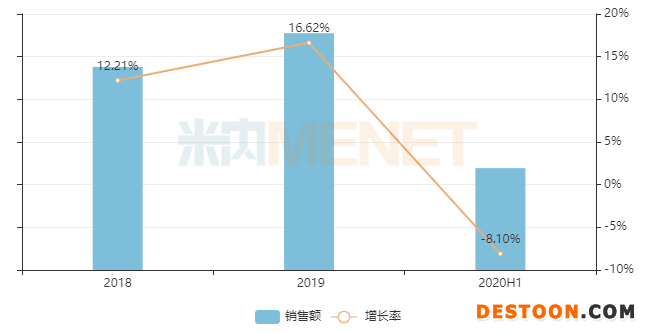
來源:米內(nèi)網(wǎng)中國公立醫(yī)療機(jī)構(gòu)終端競爭格局
米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年在中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端眼科用藥的市場規(guī)模已經(jīng)超過了百億,2017-2019年銷售額增速均超過10%,2020上半年受疫情影響下滑8.10%。TOP20企業(yè)排名,齊魯制藥排在18位,2020上半年市場份額為1.17%,比2019年上漲了0.07%。
表1:2017年至今齊魯獲批的眼科用藥上市申請情況
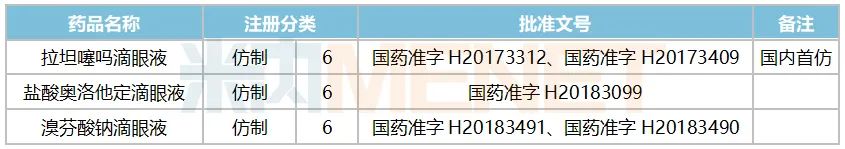
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
表2:齊魯目前在審的眼科用藥上市申請情況
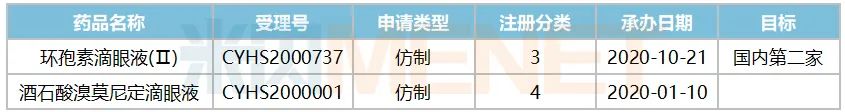
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
2017年至今,齊魯已有三大眼科用藥仿制藥獲批上市,其中拉坦噻嗎滴眼液為國內(nèi)首仿,產(chǎn)品進(jìn)入市場后原研輝瑞的市場份額下滑至2020H1的93.91%。目前,除了新申報(bào)上市的溴莫尼定噻嗎洛爾滴眼液外,齊魯仍有兩個(gè)高端仿制眼科用藥在審評審批中,涉及環(huán)孢素滴眼液(Ⅱ)以及酒石酸溴莫尼定滴眼液。
來源:CDE官網(wǎng)、米內(nèi)網(wǎng)數(shù)據(jù)庫
審評數(shù)據(jù)統(tǒng)計(jì)截至2020年11月30日,如有錯(cuò)漏,敬請指正。



 110102000668(1)號
110102000668(1)號