1月19日訊 1月18日,NMPA官網(wǎng)更新了獲批藥品信息,奧賽康的注射用替莫唑胺3類仿制上市申請(qǐng)獲批并視同過評(píng)。2019年1月,恒瑞發(fā)布公告稱公司的注射用替莫唑胺3類仿制獲批并拿下了國內(nèi)首仿。截至目前,替莫唑胺的膠囊劑與注射劑均有兩家企業(yè)過評(píng),并且口服常釋劑型已被納入第四批國家集采目錄。
圖1:奧賽康的注射用替莫唑胺獲批信息

來源:NMPA官網(wǎng)
圖2:替莫唑胺的銷售情況
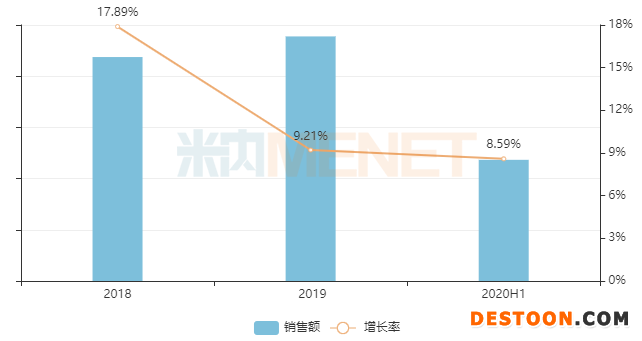
來源:米內(nèi)網(wǎng)中國公立醫(yī)療機(jī)構(gòu)終端競爭格局
據(jù)悉,替莫唑胺是一種咪唑并四嗪類具有抗腫瘤活性的烷化劑,該藥品可用于治療新診斷的多形性膠質(zhì)母細(xì)胞瘤成人患者,開始先與放療聯(lián)合治療,隨后作為維持治療;也可用于治療難治性間變性星形細(xì)胞瘤成人患者,例如用含亞硝基脲和甲基芐肼的常規(guī)方案治療后疾病進(jìn)展的患者。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2018年起在中國城市公立醫(yī)院、縣級(jí)公立醫(yī)院、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機(jī)構(gòu))終端該品種的銷售額已超過20億元,增速達(dá)17.89%,最近兩年增速有所放緩。
2019年1月4日,恒瑞發(fā)布公告稱,公司申報(bào)的注射用替莫唑胺3類仿制獲批并視同過評(píng),順利拿下國內(nèi)首仿,該產(chǎn)品項(xiàng)目投入研發(fā)費(fèi)用約679萬元。
表1:目前過評(píng)的替莫唑胺相關(guān)產(chǎn)品情況
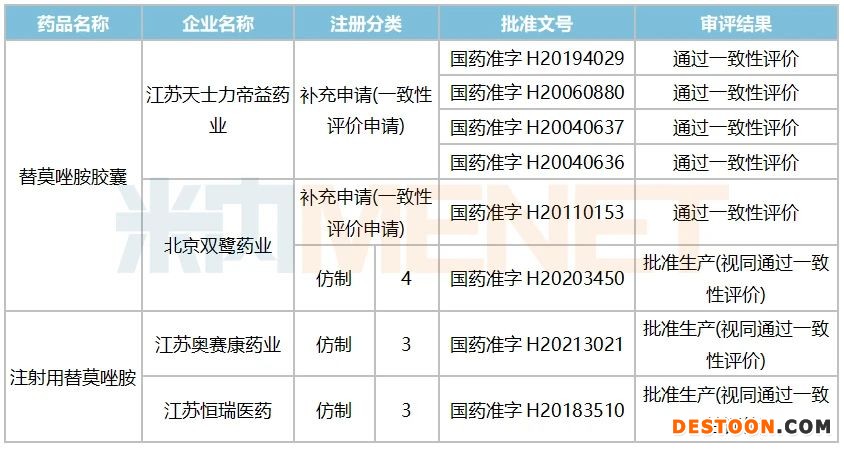
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評(píng)數(shù)據(jù)庫
目前國內(nèi)市場上的替莫唑胺有膠囊劑及注射劑獲批上市,膠囊劑過評(píng)企業(yè)有天士力、雙鷺?biāo)帢I(yè),并已被納入第四批國家集采目錄,將與原研默沙東展開價(jià)格激戰(zhàn);而注射劑除了恒瑞醫(yī)藥外,奧賽康也按新分類獲批視同過評(píng)。該產(chǎn)品同時(shí)也是奧賽康于2021年獲批的首個(gè)新品,目前該公司還有1個(gè)2.2類新藥、8個(gè)按新分類(3類、4類)申報(bào)上市的仿制藥在審評(píng)審批中。
來源:NMPA官網(wǎng)、米內(nèi)網(wǎng)數(shù)據(jù)庫
審評(píng)數(shù)據(jù)統(tǒng)計(jì)截至2021年1月18日,如有錯(cuò)漏,敬請(qǐng)指正。



